Как уничтожить опухолевые клетки рака?

Опухолевые клетки ‒ это перерожденные и мутированные по своей структуре здоровые клетки организма. Среди наиболее распространенных причин клеточной трансформации ученые выдели такие:
- Избыток белка SP2, который способствует преобразованию стволовых клеток в опухолевые.
- Вирус рака, проблемы иммунной системы, генетика и окружающая среда.
- Отсутствие конкретных взаимодействующих молекул, которые стимулируют антигены и реагируют на связь с лимфоцитами.
- Ухудшение естественных способностей клеток-киллеров, что провоцирует рак.
- Генетические изменения, вызывающие рак, могут передаваться по наследству, и провоцировать ошибки в деятельности ДНК.
Особенности опухолевой клетки
Онкологическая клетка отличается от обычной такими параметрами:
- решающую роль в оценке опухолевой клетки играет ядро. Его поверхность, форма, структура, размер, плотность и окрас изменены;
- ядрышки клеток характеризуются гипертрофией;
- атипичные митозы клетки имеют ассиметричную структуру и неправильное количество хромосом;
- ядерные аномалии приводят к образованию клеточных клонов и генетических мутаций;
- устойчивость к лекарственным препаратам за счет специфической молекулы на поверхности опухоли. Она возвращает опухолевую клетку к состоянию стволовой, что делает ее невосприимчивой к медикаментам;
- возможностью уклониться от иммунной системы, а также использовать ее, чтобы выжить и расти.
Какие свойства опухолевых клеток?
Раковые клетки характеризуются такими условиями:
- Ускорением клеточного цикла.
- Неконтролируемым миотическим делением, вызывающим неорганизованный рост тканей и их скопление в любом месте организма.
- Геномными изменениями. Опухолевые клетки отличаются от нормальных отсутствием узкой специализации и строгой функциональности. Это позволяет им беспрепятственно делиться, формируя новые ряды мутаций.
- Отказом реагировать на сигналы защитных свойств организма, в связи с чем в их структуре исчезает склонность к апоптозу (клеточной гибели).
- Трансформациями в клеточной поверхности, секреции и т. д.
- Влиянием на молекулы нормальных клеток и кровеносные сосуды. Опухолевые клетки рака способны использовать здоровые для формирования нужных кровеносных сосудов, чтобы питать микросреду онкологического образования: снабжать кислородом, питательными веществами и даже удалять ненужные злокачественным тканям элементы.
- Увеличением мобильности из-за очень малых размеров. Это позволяет опухолевым клеткам перемещаться по разным частям тела и провоцировать злокачественный рост опухолей. Это свойство является причиной метастазирования.
Важно знать: Профилактика рака. План защиты на каждый день
Что такое циркулирующие опухолевые клетки и чем они опасны?
Этим термином обозначаются раковые клетки, которые отделяются от первичного онкообразования и попадают в кровоток. Таким образом, они представляют собой “семена” для последующего роста опухоли (метастазирования).
Как правило, циркулирующие опухолевые клетки захватывают сосудистую систему с помощью специфических антител, которые распознаются опухолевым маркером EpCAM. Однако, это не всегда возможно.
Методы обнаружения циркулирующих опухолевых клеток включают:
- Использование наночастиц, покрытых полимерным слоем аналога биотина, что также сдержит EpCAM. Сначала структура всех клеток организма окрашивается в определенный цвет. После этого образец сканируется анализатором, способным выявить ядерную основу. Если общее количество клеток превышает 5, образец крови положительный.
- Технология, что базируется на отделении клетки от ядросодержащих красных кровяных клеток, которые имеют измененное ядро. Все клетки метятся люминисцентными антителами, содержащими биомаркер рака. Система визуализации захватывает около 3 миллионов клеток. А для анализа задействуется 90 различных параметров. Метод позволяет выявить около 20 видов рака.
- Применение диагностической платформы для выявления опухолевых клеток в жидкостях, а также исследование их молекулярной характеристики. Этот метод базируется на микроскопическом отделении циркулирующих опухолевых клеток и их дифференциации в сравнении с иными клетками крови.
Обязательно к прочтению: Как не заболеть раком: 10 советов
Уничтожение опухолевых клеток
Важную роль в функционировании клеточного процесса и уничтожении мутированных элементов играет иммунитет. Он предотвращает и обезвреживает опухолевые формирования. Клинические исследования показали, что активная иммунная система постоянно вычисляет и устраняет отклонения в клетках прежде, чем они образуют опухоль.
Противораковое действие иммунной системы заключается в трех основных этапах:
- Иммунитет распознает и ликвидирует опухолевые клетки рака на самых ранних стадиях.
- Иммунная система устраняет опухолевые клетки в фазе равновесия. Но на этом этапе возможно только частичное устранение мутированных тканей.
- Опухолевые клетки становятся не восприимчивыми к атакам иммунной системы. Поэтому они продолжают расти и делится.
Важно знать: Что убивает раковые клетки?
Современные методы уничтожения опухолевых клеток
Ученые исследовали главные способы выведения из строя атипичных клеток:
- Главное задание человека ‒ придерживаться здорового образа жизни и правил питания. Ученые рекомендуют принимать пищу, обогащенную витаминами, минералами и антиоксидантами. Это различные фрукты и овощи, бобовые, сложные углеводы, белое мясо и т.д. Здоровое питание поможет противостоять развитию злокачественных клеток.
- Использовать средства народной медицины и фитотерапии. Их преимущество ‒ безвредность. Также, многие растения обладают иммуностимулирующим действием, запуская защитные силы организма, а те, в свою очередь, сами предупреждают злокачественные клеточные изменения в организме.
- Опухолевые клетки рака могут быть устранены современными способами:
- ученые разработали подход, который провоцируют целевой белок распадаться. До этого он только запрещался на некоторое время, а потом снова рос. Новая технология позволяет доставить целевые препараты для уничтожения опухолевых клеток непосредственно к атипичному белку;
- иной метод использует активацию запрограммированной клеточной смерти в клетках рака. Он нацелен на применение белка Bcl-2, уже известного в лечении онкозаболеваний;
- устранение рецептора FAS, также известного как CD95 и его компонента ‒ лиганда CD. При этом способе также срабатывает клеточная функция апоптоза, что провоцирует саморазрушение опухолевой клетки.
Возможность выявить обычные мутированные опухолевые клетки и циркулирующие ‒ одна из главных задач диагностики онкологии. Не менее важным также является и исследование способов, с помощью которых происходит уничтожение опухолевых клеток.
Источник: https://orake.info/opuxolevye-kletki-kak-unichtozhit-opuxolevye-kletki-raka/
Почему возникает рак? | Глава 2 От клетки до опухоли | Читать онлайн, без регистрации
Почему возникает рак?
Поиск пускового механизма и факторов риска, приводящих к возникновению РМЖ, активно проводится многими научно-исследовательскими лабораториями, а эпидемиологические данные с каждым годом прибавляют к нашим знаниям новые факторы, которые способствуют развитию РМЖ. Однако до настоящего времени нет единого мнения о причинах этого заболевания.
Основу многих патологических процессов, в том числе и опухолей, составляет патология клетки.
Если вы помните из школьного курса биологии – клетка является структурной и функциональной единицей живых организмов, осуществляющей рост, развитие, обмен веществ и энергии, хранящей, перерабатывающей и реализующей генетическую информацию.
В нормальных условиях клетки органов и тканей определенным образом взаимодействуют между собой. Однако при опухолевом росте подобные взаимосвязи нарушаются, в результате чего опухолевые клетки почти не контактируют друг с другом и изолированы от окружающей их нормальной ткани.
По-видимому, такое состояние приводит к освобождению злокачественных клеток из-под контроля координирующих клеточную пролиферацию (размножение) факторов, которые в нормальных условиях постоянно циркулируют через межклеточные мембраны.
Проведенные исследования позволили установить, что уровень пролиферации клеток в опухолях человека не только не превышает, а часто бывает значительно ниже соответствующего показателя для нормальных (неопухолевых) тканей.
Полученные данные свидетельствуют, что опухоль растет не за счет сокращения продолжительности клеточного цикла, а благодаря тому, что воспроизводство клеток превышает клеточные потери, тогда как в нормальных тканях взрослого человека эти процессы сбалансированы.
В осуществлении контроля за активностью деления клеток ведущая роль отводится особым группам генов – протоонкогенам (контролируют нормальное клеточное деление и дифференцировку – созревание – клеток) и антионкогенам (их продукты угнетают способность клеток к размножению).
В условиях патологии (при изменениях строения ДНК или увеличении количества генов) протоонкогены могут превращаться в онкогены – гены, вызывающие злокачественную трансформацию клетки.
Таким образом может быть положено начало формирования опухолевого клона клеток. Среди антионкогенов наиболее известен ген р53.
При нарушении его функции контроль над клеточным циклом утрачивается: клетки-мутанты, несмотря на повреждения ДНК, продолжают активно пролиферировать, что приводит к появлению опухолей.
Исходя из вышеизложенного, процесс развития новообразований в общем виде можно представить следующим образом: под влиянием какого-либо неблагоприятного фактора происходит нелетальное повреждение генома (генетического аппарата) клетки, в результате чего наблюдается активация онкогенов или подавление антионкогенов, приводящее к воспроизводству продуктов измененных генов и утрате продуктов регуляторных генов, способствующее формированию клона измененных (мутантных) клеток и возникновению опухоли.
Единого, общепринятого определения опухолевого процесса нет до настоящего времени, что, по-видимому, объясняется сложностью и многообразием злокачественных новообразований, а также отсутствием полных сведений о природе рака.
Согласно современным представлениям, опухоль – это патологический процесс, представленный новообразованной тканью, в которой изменения генетического аппарата клеток приводят к нарушению регуляции их роста и дифференцировки.
Факторами, вызывающими генетические повреждения клеток и их злокачественную трансформацию, могут являться химические (полициклические углеводороды, нитрозосоединения, тяжелые металлы и др.) или физические (различные виды ионизирующей радиации, ультрафиолетовое излучение и др.) канцерогены и онкогенные (способствующие возникновению опухолей) вирусы.
Злокачественные (малигнизированные) клетки отличаются от нормальных, окружающих их клеток тем, что способны:
– вырабатывать вещества, обеспечивающие им автономность бесконечного роста, независимого от факторов, регулирующих в организме деление клеток;
– обеспечивать себе преимущества выживания за счет изменения в клетке обмена углеводов, белков, жиров, повышенного поглощения необходимых для роста соединений из здоровых тканей;
– накапливать воду и некоторые электролиты;
– утрачивать признаки внутриклеточной организации, свойственные здоровым клеткам данного органа или ткани;
– приобретать структурные комплексы (антигены), отсутствующие у нормальных клеток, или терять уже существующие (антигенное упрощение).
Биологическими особенностями злокачественной опухоли являются:
– инфильтративный рост – проникновение опухолевых клеток в окружающие ткани с их деструкцией (разрушением). В отличие от этого доброкачественные опухоли только сдавливают и отодвигают окружающие ткани, но не прорастают в них;
– метастазирование – перенос опухолевых клеток за пределы первичной опухоли в различные органы и ткани с образованием вторичных опухолевых узлов той же гистологической (тканевой) структуры;
– рецидивирование – возникновение опухоли на том же самом месте после ее хирургического удаления или излечения с помощью лучевой или химиотерапии.
Причинами подобного явления могут быть сохранившиеся в оставленной части органа условия, благоприятствующие возникновению новой опухоли на фоне прогрессирующих пред-опухолевых заболеваний, понижение сопротивляемости организма (иммунодепрессия) и другие факторы;
– кахексия – синдром истощения и слабости организма, сопровождающийся отвращением к пище и изменением вкусовых ощущений, чаще всего наблюдается при новообразованиях желудочно-кишечного тракта.
Большинство опухолей человека происходит из постоянно обновляющихся тканей. Обновление тканей в нормальных условиях связано с делением и созреванием небольшого числа особых клеток, получивших название стволовых.
Стимулом доя этих процессов является необходимость замещения погибших клеток, приспособленных к выполнению строго специализированных функций. Таким образом обеспечивается поддерживание постоянства характеристик той или иной ткани.
Доказано, что при определенных условиях нормальная стволовая клетка может порождать злокачественную.
На ранних стадиях развития новообразования подавляющее большинство малигнизированных клеток участвует в процессе деления.
По мере роста опухоли происходят стойкие качественные изменения ее свойств в сторону повышения злокачественности, что может быть связано с отбором определенных клеточных клонов, а также с изменениями, происходящими в самих опухолевых клетках.
Число клеток, составляющих пролиферативный пул, уменьшается и к моменту клинического диагноза не превышает 20 % от их общего количества в опухоли.
Промежуток времени от начала трансформации нормальной клетки до первых клинических проявлений заболевания может составлять 10–12 лет.
Но существуют и стремительно растущие опухоли, характеризующиеся высокой интенсивностью деления клеток и соответственно значительно более ранними проявлениями симптомов болезни. На них приходится 1/5 часть всех случаев РМЖ.
Темп клинического течения новообразования зависит от доли клеток опухоли, участвующих в пролиферации, а также величины клеточных потерь (гибели злокачественных клеток).
Оба этих фактора определяются степенью васкуляризации (развития сосудов) опухоли. Известно, что малигнизированные клетки способны выделять факторы, способствующие развитию в опухоли кровеносных сосудов.
Биологически активные вещества, обладающие подобным действием, могут вырабатывать и макрофаги (клетки соединительной ткани, способные к захватыванию и перерабатыванию посторонних организму частичек), проникающие в опухолевую ткань.
Согласно современным представлениям в развитии опухолей выделяют три разные, но часто накладывающиеся друг на друга фазы:
– инициацию (опухолевую трансформацию) – первый шаг, сущность которого составляет быстрое и необратимое изменение на генетическом уровне в виде мутации (стойкого изменения) ДНК – наследственной структуры, ответственной за хранение генетической информации и передачи ее от клетки к клетке. Однако трансформированные таким образом клетки остаются неактивными без дополнительных стимулов к делению и процесс может оборваться;
– промоция – следующий шаг, заключающийся во взаимодействии между трансформированной клеткой и рядом биологически активных веществ, в результате которого происходит отбор клеток с высокой репродуктивной активностью и образуется достаточно обширный клон измененных клеток, т. е. формируется первичный опухолевой узел;
– прогрессия – еще один шаг, включающий возникновение дополнительных изменений в структуре генома и отбор клеточных клонов, наиболее приспособленных к меняющимся условиям существования, а следовательно наиболее агрессивных в отношении организма хозяина. Считается, что на этом этапе опухоль приобретает истинные признаки злокачественности – способность к инфильтрирующему росту и метастазированию.
Таким образом, формирование злокачественного новообразования не одноразовое событие, а цепь последовательных взаимосвязанных изменений, каждое из которых обусловлено воздействием внешних и внутренних факторов.
«Но что же организм? – спросите вы. – Неужели он не может сопротивляться злокачественному росту?» Напротив, существует особая система, обеспечивающая генетическое постоянство внутренней среды организма, вылавливающая чужеродные, измененные клетки. Это система иммунитета.
Впечатляет один только перечень органов иммунитета: костный мозг, фабрициева сумка (у птиц, у человека ее аналог не выявлен), лимфатические узлы, селезенка, кожа и субэпителиальная лимфоидная ткань слизистых оболочек.
В костном мозге осуществляются очень важные процессы, называемые кроветворением.
Как известно, в крови выявлено три главных вида клеток: эритроциты – «красные кровяные шарики», переносящие кислород, лейкоциты – «белые кровяные шарики» – «солдаты» системы иммунитета и тромбоциты, отвечающие за свертываемость крови.
Разновидностью лейкоцитов являются лимфоциты, среди которых выделены Т– и В-клетки. Т-лимфоциты отвечают за клеточный иммунитет, направленный на отторжение чужеродного трансплантата. Они проходят «обучение» в тимусе, где подвергаются дифференцировке на Т-лимфоциты-помощники (Т-хелперы), Т-лимфоциты-подавители (Т-супрессоры) и Т-лимфоциты-убийцы (Т-киллеры).
В-лимфоциты отвечают за гуморальный иммунитет, несут функции антителообразования, направленные на уничтожение всего чужеродного организму. Они «живут» в костном мозге, селезенке, «заходят» в лимфатические узлы, а вот в тимусе их нет.
В лимфатическом и кровяном русле Т– и В-клетки встречаются и взаимодействуют. Поводом для этого служит внедрение любого чужеродного агента или появление собственной трансформированной клетки.
Получив соответствующий сигнал, В-лимфоциты превращаются в плазматические клетки, начинается продукция антител (иммуноглобулинов). Т-хелперы активно способствуют этому процессу. Когда антител накопилось достаточно, Т-супрессоры останавливают их выработку.
Т-киллеры выслеживают клетки с «чужим» генетическим кодом и немедленно с ними расправляются.
Важную роль в иммунных реакциях играют макрофаги. Они подают чужеродный антиген лимфоцитам. В организации иммунного ответа на чужеродный агент принимают также участие различные биологически активные вещества – интерлейкины, интерфероны и другие.
Однако такая достаточно сложная цепь развития иммунных реакций, хоть и представленная схематично, разворачивается только в том случае, если внедрившийся агент не может быть уничтожен на первой линии иммунной защиты – в системе естественной неспецифической резистентности.
Она способна самостоятельно разрушать небольшое количество опухолевых клеток.
В организме эта система представлена макрофагами, естественными киллерами – особыми лимфоцитами, не зависящими от тимуса, способными в течение 1–2 часов убивать клетки-мишени без предварительной подготовки в виде иммунного ответа.
Сюда же относится система комплемента – комплекс белков, работающий по принципу каскада последовательно активизируемых факторов. Она ускоряет поглощение чужеродных агентов фагоцитами (от греческого слова фагос – пожиратель). В первой линии защиты участвуют также различные биологически активные вещества, образующиеся в организме.
Существуют и другие механизмы противоопухолевой резистентности (сопротивляемости), в том числе препятствующие контакту канцерогенов (веществ, способствующих возникновению злокачественных опухолей) с клетками и внутриклеточными структурами, трансформации нормальной клетки в опухолевую, а также неиммуногенные механизмы, противодействующие формированию из образовавшихся отдельных клеток колонии – опухоли.
Далеко не всякий возникший в организме клон малигнизированных клеток превращается в злокачественную опухоль. Однако если система антибластомной резистентности не справляется с возложенными на нее задачами, опухолевые клетки не только сохраняются, но из них развивается опухоль. Причинами этого являются:
1. Подавление защитных сил организма, их неспособность дать адекватный иммунный ответ на наличие злокачественной клетки, вследствие:
– воздействия канцерогенных факторов;
– влияния самого злокачественного новообразования;
– сопутствующих хронических заболеваний;
– нерационального питания;
– врожденных дефектов иммунной системы;
– приема некоторых лекарственных препаратов;
– регулярных продолжительных стрессов.
2. Нарушение нормального функционирования нервных клеток, приводящее к изменениям в энергетическом, белковом и углеродном обменах, необходимых для формирования опухолевого узла, а также к нарушениям механизмов регуляции генетического аппарата клетки.
3. Наличие в организме эндокринного дисбаланса, в результате чего:
– повышается способность к размножению клеток тканей – мишеней действия соответствующего гормона;
– возрастает возможность повреждения генетического аппарата делящихся клеток с их последующей злокачественной трансформацией;
– изменяется обмен канцерогенов;
– нарушается способность организма удалять трансформированные клетки.
Препятствуют уничтожению и способствуют сохранению опухолевых клеток и ряд других факторов, в том числе особенности строения клеточных структур (антигенов), позволяющие злокачественным клеткам ускользать от иммунного контроля.
Источник: http://velib.com/read_book/aljasova_anna_valerevna/zabolevanija_molochnojj_zhelezy_profilaktika_i_metody_lechenija/glava_2_ot_kletki_do_opukholi/pochemu_voznikaet_rak/
Клетки злокачественных опухолей
Клетки злокачественного образования существуют в организме у каждого человека в виду постоянных мутационных процессов. Однако при нормальном функционировании иммунной системы происходит своевременное уничтожение данных патогенов.
При сбое в иммунитете свойства клеток рака позволяют им обмануть хелперы и выжить, тем самым начиная процесс уничтожения макроорганизма. Все клетки злокачественных опухолей подразделяются на виды, современная статистика рака говорит о том, что далеко не все они одинаково опасны для здоровья и жизни человека.
Обо всех различиях и свойствах данных образований можно узнать из предлагаемого материала.
Опухолевые клетки рака в организме: их активность и уничтожение
Человеческий организм состоит из миллионов клеток, каждая из которых обладает определенными функциями. Нормальные клетки растут, делятся и умирают в определенной закономерности. Этот процесс строго контролируется организмом. Скорость деления клеток различна в разных органах и тканях.
В тех случаях, когда структура клеток меняется под воздействием различных факторов: экология, радиационный фон, неправильное питание, стрессы, вредные привычки, наследственность — все эти факторы воздействуют на каждого по-разному.
Опухолевые клетки рака начинают делиться бесконтрольно, теряют способность распознавать свои клетки и структуры и становятся раковыми клетками, они формируют опухоль и могут проникать в другие органы и ткани, нарушая их функции.
Почти все опухоли развиваются в нормальных тканях организма, и чаще в тех тканях и органах, в которых скорость деления клеток выше.
Опухолевые клетки в организме отличаются от нормальных клеток тем, что вместо гибели они продолжают расти и делиться, образовывать новые патологические. Патология — болезненное отклонение от нормального состояния или процесса развития.
Активность опухолевых клеток заключается в том, что они обычно вырабатывают токсические вещества, которые приводят к ухудшению состояния человека, слабости, потере аппетита и похудению. Простая опухоль называется доброкачественной, она просто растет снаружи органа.
Доброкачественная опухоль может вырасти до больших размеров и передавить жизненно важные органы. Такую опухоль можно вырезать и забыть про нее.
Уничтожение опухолевых клеток методом удаления не эффективно при злокачественных новообразованиях, поскольку идет диссеминированное распространение по всему организму.
Свойства и особенности деления опухолевых клеток при злокачественном росте и перерождении
Совершенно другая ситуация возникает в случае, когда, помимо способности чрезмерно размножаться, мутировавшие клетки приобретают вредные особенности опухолевых клеток — проникать сквозь слои других клеток.
Такая опухоль не просто увеличивается в размерах, но еще и прорастает сквозь другие органы и ткани. Когда масса при делении опухолевых клеток тянется сквозь здоровую ткань, она образует лучи, иногда похожие на клешни рака.
Это сравнение послужило основой для такого названия, как рак. Рак является злокачественной опухолью.
Неконтролируемое деление опухолевых клеток может также привести к доброкачественной опухоли. Доброкачественные опухоли отличаются тем, что не образуют метастазов, не вторгаются в другие ткани и потому редко опасны для жизни.
Однако доброкачественные опухоли часто превращаются в злокачественные (перерождение клеток в злокачественных происходит под влиянием негативных факторов).
Токсические свойства опухолевых клеток подавляют иммунитет и человек становится абсолютно беззащитным перед онкологией.
Окончательный диагноз злокачественной опухоли ставится после гистологического исследования образца ткани патоморфологом. Для того чтобы подавить злокачественный рост клеток, после диагностики назначается оперативное лечение, химиотерапия и лучевая терапия. По мере совершенствования медицинской науки лечение становится все более специфичным для каждого вида опухолей.
Злокачественные опухоли поражают людей всех возрастов, но гораздо чаще возникают в пожилом возрасте. Это одна из основных причин смерти в развитых странах. Появление многих опухолей связано с действием факторов окружающей среды, таких как алкоголь, табачный дым, ионизирующее излучение, некоторые вирусы.
Существует множество видов злокачественных опухолей, которые классифицируются в зависимости от органа, в котором появилась первичная опухоль, типа клеток, которые претерпевают раковую трансформацию, а также клинических симптомов, наблюдаемых у пациента.
Область медицины, занимающаяся изучением и лечением злокачественных опухолей, называется онкологией.
Свойства онкологических клеток
- Склонность к быстрому неконтролируемому росту, носящему разрушительный характер и приводящему к сдавлению и повреждению окружающих нормальных тканей.
- Склонность к проникновению (инвазии, инфильтрации, пенетрации) в окружающие ткани, с формированием местных метастазов.
- Склонность к метастазированию в другие, часто весьма отдаленные от исходной опухоли ткани и органы посредством перемещения по лимфо- и кровеносным сосудам, а также имплантационно. Причем определенные типы опухолей проявляют определенное родство (тропность) к определенным тканям и органам — метастазируют в определенные места (но могут метастазировать и в другие).
- Наличие выраженного общего влияния на организм вследствие выработки опухолью токсинов, подавляющих противоопухолевый и общий иммунитет, способствующих развитию у больных общего отравления (интоксикации), физического истощения (астении), депрессии, исхудания вплоть до так называемой кахексии.
- Способность к ускользанию от иммунологического контроля организма при помощи специальных механизмов обмана Т-киллерных клеток.
- Наличие в опухолевых клетках значительного числа мутаций, число которых увеличивается вместе с возрастом и массой опухоли; некоторые из этих поломок необходимы для собственно канцерогенеза, некоторые необходимы для ускользания от иммунитета или для приобретения способности к метастазированию, другие же случайны и возникают вследствие пониженной устойчивости опухолевых клеток к повреждающим воздействиям.
- Незрелость (недифференцированность) или низкая по сравнению с доброкачественными опухолями степень зрелости составляющих опухоль клеток. Причем чем ниже степень зрелости клеток, тем злокачественнее опухоль, тем быстрее растет и раньше метастазирует, но зато, как правило, тем чувствительнее она к лучевой и химиотерапии.
- Наличие выраженной тканевой и/или клеточной ненормальности (атипизма).
- Преобладание клеточного атипизма над тканевым.
- Интенсивная стимуляция роста кровеносной системы (ангиогенез) в опухоли, приводящая к ее наполнению кровеносными сосудами (васкуляризации) и часто к кровоизлияниям в ткань опухоли.
Виды злокачественных опухолей различаются по типу клеток, из которых они возникают:
- карцинома, или собственно рак — из эпителиальных клеток (например, рак предстательной железы, легких, молочной железы, прямой кишки);
- меланома — из меланоцитов;
- саркома — из соединительной ткани, костей и мышц (мезенхима);
- лейкоз — из стволовых клеток костного мозга — важнейшего органа кроветворной системы, продуцирующей клетки крови;
- лимфома — из лимфатической ткани;
- тератома — из зародышевых клеток;
- глиома — из глиальных клеток;
- хориокарцинома — из ткани плаценты.
Существуют типы злокачественных опухолей, особенно часто поражающие детей и подростков. Заболеваемость детей злокачественными опухолями наиболее высока в первые 5 лет жизни.
Среди опухолей лидируют лейкозы (особенно острый лимфобластный лейкоз), опухоли центральной нервной системы и нейробластома.
Далее следуют нефробластома (опухоль Вильмса), лимфомы, рабдомиосаркома, ретинобластома, остеосаркома и саркома Юинга.
Статья прочитана 3 423 раз(a).
Источник: http://med-pomosh.com/?p=6580
Уничтожить рак помогут злокачественные клетки
В исследовательском институте Скриппса команда ученых нашла способ лечения лейкемии. После нескольких лет работы ученые обнаружили способ, как заставить раковые клетки уничтожать себе подобных.
Данное открытие может стать настоящим прорывом в медицине и помочь в лечении не только лейкоза, но и других раковых заболеваний.
Группа специалистов в начале работы занималась поиском антител, которые могли запускать рецепторы роста на клетках костного мозга, которые находятся в незрелом состоянии.
Как предполагают ученые, такой механизм помог бы преобразовать незрелые клетки костного мозга в клетки крови. Но также специалисты отметили, что некоторые антитела могут оказать непредсказуемый эффект на клетки костного мозга и превратить их в любые типы клеток, к примеру, в нервные.
Открытие натолкнуло ученых на мысль, возможно ли при помощи такого метода превратить атипичные клетки в нормальные. В результате было проверено 20 антител, которые активируют рецепторы на лейкозных клетках и только один из них оказался действующим.
Антитела производили на лейкозные клетки человека исключительный эффект – преобразовывали их в ключевые клетки иммунной системы, при увеличении времени воздействия ключевые клетки становились NK-клетками, которые отличаются быстротой реакции на различные патологические процессы в организме. Такие клетки эффективно противостоят не только вирусам и бактериям, но и раковым клеткам.
Результаты экспериментов оказались довольно впечатляющими – небольшое количество NK-клеток за сутки уничтожило около 15% лейкозных клеток, которые их окружали.
Авторы исследовательского проекта д-р Лита Анненберг и д-р Ричард Лернер отметили, что результаты их работы станут новым этапом в лечении разных раковых заболеваний.
Рак является наиболее страшной и опасной болезнью человечества, ежегодно от разных видов онкологии умирает огромное количество человек, и ученые по всему миру пытаются найти способ лечения раковых заболеваний.
Так, в одном из крупнейших частных медицинских центров мира, клинике Майо, команда специалистов разработала способ, чтобы вернуть атипичные клетки в нормальное состояние.
Новый метод оказался эффективным и помог в лечении некоторых видов рака.
Глава научного проекта Панагиотис Анастасиадисон отметил, его группа смогла сделать так, чтобы остановился рост опухоли, и атипичные клетки вернулись к нормальному состоянию.
В ходе своей работы ученые использовали ген Plekha7, который продуцирует белок, оказывающий влияние на неправильные клетки. Этот белок не позволяет клеткам делиться и перерастать в злокачественную опухоль.
Исследователи проводили испытание новой методики на нескольких агрессивных формах онкологических опухолей, и результаты оказались положительными.
Анастасиадисон пояснил, что смогла понять принципа развития раковых опухолей и подобрать «ключ» к новообразованиям.
Сейчас ученые находятся на завершающем этапе, в будущем новую методику планируется применять для лечения раковых опухолей груди, мочевого пузыря и легких.
Источник: https://ilive.com.ua/news/unichtozhit-rak-pomogut-zlokachestvennye-kletki_94166i15817.html
Одураченные макрофаги, или несколько слов о том, как злокачественные опухоли обманывают иммунитет
Статья на конкурс «био/мол/текст»: Иммунная система — это мощная многослойная защита нашего организма, которая потрясающе эффективна против вирусов, бактерий, грибов и других патогенов извне.
Кроме того, иммунитет способен эффективно распознавать и уничтожать трансформированные собственные клетки, которые могут перерождаться в злокачественные опухоли. Однако сбои в работе иммунной системы (по генетическим либо другим причинам) приводят к тому, что однажды злокачественные клетки берут верх.
Разросшаяся опухоль становится нечувствительной к атакам организма и не только успешно избегает уничтожения, но и активно «перепрограммирует» защитные клетки для обеспечения собственных нужд.
Поняв механизмы, которые опухоль использует для подавления иммунного ответа, мы сможем разработать контрмеры и попытаться сдвинуть баланс в сторону активации собственных защитных сил организма для борьбы с болезнью.
Долгое время считалось, что причина низкой эффективности иммунного ответа при раке — то, что опухолевые клетки слишком похожи на нормальные, здоровые, чтобы иммунная система, настроенная на поиск «чужаков», могла их как следует распознавать. Этим как раз и объясняется тот факт, что иммунная система успешнее всего противостоит опухолям вирусной природы (их частота резко возрастает у людей, страдающих иммунодефицитом). Однако позже стало ясно, что это не единственная причина.
Оказалось, что взаимодействие раковых клеток с иммунной системой носит гораздо более разносторонний характер. Опухоль не просто «прячется» от атак, она умеет активно подавлять местный иммунный ответ и перепрограммировать иммунные клетки, заставляя их обслуживать собственные злокачественные нужды.
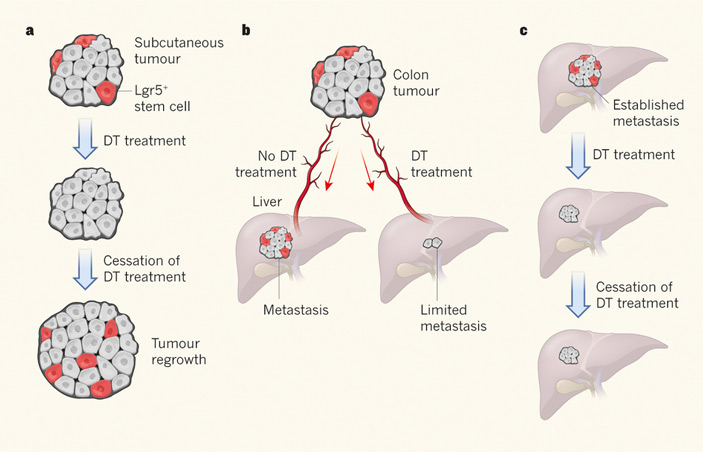
«Диалог» между переродившейся, вышедшей из-под контроля клеткой с ее потомством (то есть будущей опухолью) и организмом развивается в несколько стадий, и если вначале инициатива почти всецело находится на стороне защитных сил организма, то в конце (в случае развития болезни) — переходит на сторону опухоли. Несколько лет назад учеными-онкоиммунологами была сформулирована концепция «иммуноредактирования» (immunoediting), описывающая основные этапы этого процесса (рис. 1) [2].
Рисунок 1. Иммуноредактирование (immunoediting) в процессе развития злокачественной опухоли.
Первая стадия иммуноредактирования — процесс устранения (elimination).
Под действием внешних канцерогенных факторов или в результате мутаций нормальная клетка «трансформируется» — приобретает способность неограниченно делиться и не отвечать на регуляторные сигналы организма. Но при этом она, как правило, начинает синтезировать на своей поверхности особые «опухолевые антигены» и «сигналы опасности».
Эти сигналы привлекают клетки иммунной системы, прежде всего макрофаги, натуральные киллеры и Т-клетки. В большинстве случаев они успешно уничтожают «испортившиеся» клетки, прерывая развитие опухоли.
Однако иногда среди таких «предраковых» клеток оказывается несколько таких, у которых иммунореактивность — способность вызывать иммунный ответ — по каким-то причинам оказывается ослабленной, они синтезируют меньше опухолевых антигенов, хуже распознаются иммунной системой и, пережив первую волну иммунного ответа, продолжают делиться.
В этом случае взаимодействие опухоли с организмом выходит на вторую стадию, стадию равновесия (equilibrium). Здесь иммунная система уже не может полностью уничтожить опухоль, но еще в состоянии эффективно ограничивать ее рост.
В таком «равновесном» (и не обнаруживаемом обычными методами диагностики) состоянии микроопухоли могут существовать в организме годами.
Однако такие затаившиеся опухоли не статичны — свойства составляющих их клеток постепенно меняются под действием мутаций и последующего отбора: преимущество среди делящихся опухолевых клеток получают такие, которые способны лучше противостоять иммунной системе, и в конце концов в опухоли появляются клетки-иммуносупрессоры. Они в состоянии не только пассивно избегать уничтожения, но и активно подавлять иммунный ответ. По сути, это эволюционный процесс, в котором организм невольно «выводит» именно тот вид рака, который его убьет.
Этот драматический момент знаменует собой переход опухоли к третьей стадии развития — избегания (escape), — на которой опухоль уже малочувствительна к активности клеток иммунной системы, более того — обращает их активность себе на пользу.
Она принимается расти и метастазировать.
Именно такая опухоль обычно диагностируется медиками и изучается учеными — две предыдущие стадии протекают скрыто, и наши представления о них основаны главным образом на интерпретации целого ряда косвенных данных.
Дуализм иммунного ответа и его значение в канцерогенезе
Существует множество научных статей, описывающих, как иммунная система борется с опухолевыми клетками, но не меньшее количество публикаций демонстрирует, что присутствие клеток иммунной системы в ближайшем опухолевом окружении является негативным фактором, коррелирующим с ускоренным ростом и метастазированием рака [2], [3]. В рамках концепции иммуноредактирования, описывающей, как изменяется характер иммунного ответа по мере развития опухоли, подобное двойственное поведение наших защитников получило, наконец, свое объяснение.
Переориентирование иммунной системы от борьбы с опухолью на ее защиту возможно благодаря пластичности клеток этой системы. Говоря об иммунном ответе, мы, как правило, используем «воинственные» метафоры — «борьба», «уничтожение», «подавление».
Но мало уничтожить врага, будь то вирус, бактерия или другой паразит. Организм должен еще и исправить причиненные им повреждения.
Регенерация поврежденных тканей и заживление ран тоже находятся под контролем клеток иммунной системы: она не только «воин», но еще и «целитель».
Коварство рака заключается в том, что, будучи по сути «чужеродным агентом» в организме, он выделяет специальные вещества, которые подавляют активный иммунный ответ и побуждают лейкоциты воспринимать опухоль не как врага, требующего уничтожения, а как рану, требующую помощи, защиты и исцеления.
Мы рассмотрим некоторые механизмы того, как это происходит, на примере макрофагов. Похожие приемы опухоль использует и для того, чтобы обманывать другие клетки врожденного и приобретенного иммунитета.
Макрофаги — «клетки-воины» и «клетки-целители»
Макрофаги, пожалуй, самые знаменитые клетки врожденного иммунитета — именно с изучения их способностей к фагоцитозу Мечниковым и началась классическая клеточная иммунология.
В организме млекопитающих макрофаги — боевой авангард: первыми обнаруживая врага, они не только пытаются уничтожить его собственными силами, но также привлекают к месту сражения другие клетки иммунной системы, активируя их.
А после уничтожения чужеродных агентов принимаются активно участвовать в ликвидации причиненных повреждений, вырабатывая факторы, способствующие заживлению ран. Эту двойственную природу макрофагов опухоли используют себе на пользу.
В зависимости от преобладающей активности различают две группы макрофагов: М1 и М2.
М1-макрофаги (их еще называют классически активированными макрофагами) — «воины» — отвечают за уничтожение чужеродных агентов (в том числе и опухолевых клеток), как напрямую, так и за счет привлечения и активации других клеток иммунной системы (например, Т-киллеров). М2 макрофаги — «целители» — ускоряют регенерацию тканей и обеспечивают заживление ран [4], [8].
Присутствие в опухоли большого количества М1-макрофагов тормозит ее рост [5], а в некоторых случаях может вызвать даже практически полную ремиссию (уничтожение). И наоборот: М2-макрофаги выделяют молекулы — факторы роста, которые дополнительно стимулируют деление опухолевых клеток, то есть благоприятствуют развитию злокачественного образования.
Экспериментально было показано, что в опухолевом окружении обычно преобладают именно М2-клетки («целители»).
Хуже того: под действием веществ, выделяемых опухолевыми клетками, активные М1-макрофаги «перепрограммируются» в М2-тип [6], перестают синтезировать антиопухолевые цитокины, такие как интерлейкин-12 (IL12) или фактор некроза опухолей (TNF) и начинают выделять в окружающую среду молекулы, ускоряющие рост опухоли и прорастание кровеносных сосудов, которые будут обеспечивать ее питание, например фактор роста опухолей (TGFb) и фактор роста сосудов (VGF). Они перестают привлекать и инициировать другие клетки иммунной системы и начинают блокировать местный (противоопухолевый) иммунный ответ (рис. 2).
Рисунок 2. М1- и М2-макрофаги: их взаимодействие с опухолью и другими клетками иммунной системы.
Ключевую роль в этом перепрограммировании играют белки семейства NF-kB [7].
Эти белки являются транскрипционными факторами, контролирующими активность множества генов, необходимых для М1 активации макрофагов.
Наиболее важные представители этого семейства — р65 и р50, вместе образующие гетеродимер р65/р50, который в макрофагах активирует множество генов, связанных с острым воспалительным ответом, таких как TNF, многие интерлейкины, хемокины и цитокины.
Экспрессия этих генов привлекает все новые и новые иммунные клетки, «подсвечивая» для них район воспаления. В то же время другой гомодимер семейства NF-kB — р50/р50 — обладает противоположной активностью: связываясь с теми же самыми промоторами, он блокирует их экспрессию, снижая градус воспаления.
И та, и другая активность NF-kB транскрипционных факторов очень важна, но еще важнее равновесие между ними. Было показано, что опухоли целенаправленно выделяют вещества, которые нарушают синтез p65 белка в макрофагах и стимулируют накопление ингибиторного комплекса р50/р50 [7].
Таким способом (помимо еще ряда других) опухоль превращает агрессивных М1-макрофагов в невольных пособников своего собственного развития: М2-тип макрофагов, воспринимая опухоль как поврежденный участок ткани, включают программу восстановления, однако секретируемые ими факторы роста только добавляют ресурсы для роста опухоли.
На этом цикл замыкается — растущая опухоль привлекает новые макрофаги, которые перепрограммируются и стимулируют ее рост вместо уничтожения.
Реактивация иммунного ответа — актуальное направление антираковой терапии
Таким образом, в ближайшем окружении опухолей присутствует сложная смесь молекул: как активирующих, так и ингибирующих иммунный ответ. Перспективы развития опухоли (а значит, перспективы выживания организма) зависят от баланса ингредиентов этого «коктейля».
Если будут преобладать иммуноактиваторы — значит, опухоль не справилась с задачей и будет уничтожена или ее рост сильно затормозится. Если же преобладают иммуносупрессорные молекулы — это значит, что опухоль смогла подобрать ключ и начнет быстро прогрессировать.
Понимая механизмы, которые позволяют опухолям подавлять наш иммунитет, мы сможем разработать контрмеры и сдвинуть баланс в сторону уничтожения опухолей [8].
Как показывают эксперименты, «перепрограммирование» макрофагов (и других клеток иммунной системы) обратимо.
Поэтому одним из перспективных направлений онко-иммунологии на сегодняшний день является идея «реактивации» собственных клеток иммунной системы пациента с целью усиления эффективности других методов лечения.
Для некоторых разновидностей опухолей (например, меланом) это позволяет добиться впечатляющих результатов.
Другой пример, обнаруженный группой Меджитова [9], — обычный лактат, молекула, которая производится при недостатке кислорода в быстрорастущих опухолях за счет эффекта Варбурга [10]. Эта простая молекула стимулирует перепрограммирование макрофагов, заставляя их поддерживать рост опухоли. Лактат транспортируется внутрь макрофагов через мембранные каналы, и потенциальная терапия заключается в блокировке этих каналов.
Развитие методов антираковой терапии в настоящее время идет по нескольким направлениям сразу , и все они важны. Ведь научившись управлять иммунным ответом так же эффективно, как это делают злокачественные опухоли, мы сумеем окончательно «переиграть» эту болезнь, которая остается одной из главных причин смертности в России и в мире.
- Страшней клешней на свете нет…;
- Schreiber R.D., Old L.J., Smyth M.J. (2011). Cancer immunoediting: integrating immunity’s roles in cancer suppression and promotion. Science. 331, 1565–1570;
- Hanahan D. and Weinberg R.A. (2011). Hallmarks of cancer: the next generation. Cell. 144, 646–674;
- Martinez F.O. and Gordon S. (2014). The M1 and M2 paradigm of macrophage activation: time for reassessment. F1000Prime Rep. 6, 13;
- Ma J., Liu L., Che G., Yu N., Dai F., You Z. (2010). The M1 form of tumor-associated macrophages in non-small cell lung cancer is positively associated with survival time. BMC Cancer. 10, 112;
- Hagemann T., Wilson J., Burke F., Kulbe H., Li N.F., Plüddemann A. et al. (2006). Ovarian cancer cells polarize macrophages toward a tumor-associated phenotype. J. Immunol. 176, 5023–5032;
- Mantovani A. and Sica A. (2010). Macrophages, innate immunity and cancer: balance, tolerance, and diversity. Curr. Opin. Immunol. 22, 231–237;
- Biswas S.K. and Mantovani A. (2010). Macrophage plasticity and interaction with lymphocyte subsets: cancer as a paradigm. Nat. Immunol. 11, 889–896;
- Толл-подобные рецепторы: от революционной идеи Чарльза Джейнуэя до Нобелевской премии 2011 года;
- Colegio O.R., Chu N.Q., Szabo A.L., Chu T., Rhebergen A.M., Jairam V. et al. (2014). Functional polarization of tumour-associated macrophages by tumour-derived lactic acid. Nature. 513, 559–563;
- Как распознать рак при помощи биомаркеров?;
- Биоинформатика: Большие БД против «большого Р».
Источник: https://biomolecula.ru/articles/odurachennye-makrofagi-ili-neskolko-slov-o-tom-kak-zlokachestvennye-opukholi-obmanyvaiut-immunitet
Что такое метастазы и почему клетки опухоли бессмертны
С чего все начинается
Если вдуматься, «иммунитет пропустил раковые клетки, и из них после развилась опухоль» — вовсе не ответ на вопрос, почему начинается рак. Ведь непонятно, почему клетка вообще становится раковой.
Однозначного ответа на этот вопрос у ученых, к сожалению, нет.
Описать поведение уже имеющихся опухолей существенно проще, чем зафиксировать тот момент, когда нормальная здоровая клетка «сворачивает на кривую дорожку».
Строго говоря, такого момента и нет: в каждой живой клетке непрерывно идет множество химических процессов (завораживающая мысль, если вдуматься). Какие-то из них под влияением химических или физических факторов, могут пойти неправильно — и тогда в клетке возникают мутации.
Впрочем, мутации могут передаваться и по наследству. Далеко не все из них вызывают превращение клетки в раковую — чаще всего мутантная клетка просто гибнет — совершив самоубийство под названием «апоптоз» или дождавшись киллеров, состоящих на службе у иммунной системы.
Но в ряде случаев как раз из таких неправильных клеток вырастает опухоль.
Опухоль имеет ряд отличий от здоровой ткани, окружающей ее. Здоровые ткани в организме человека появляются и растут, подчиняясь определенным законам. Опухоль же растет просто потому что она может. Вторая ключевая особенность, пожалуй, выглядит еще более впечатляюще — клетки опухоли фактически бессмертны.
Здоровые клетки делятся определенное количество раз, после чего «кончают жизнь самоубийством» — этот принцип называется лимитом Хейфлика. У разных типов клеток он разный, но этот генетический механизм работает практически для всех здоровых клеток. А вот для опухолевых — не работает, и поэтому они способны делиться бесконечное количество раз.
Существует даже довольно иезуитская теория о том, что, поняв механизмы роста опухолей, можно найти ключ к бессмертию.
Добрые и злые
Надо отметить, что не все опухоли одинаково страшны — их обычно делят на доброкачественные и злокачественные. Первые называются так, потому что они живут в своем «гетто» — вокруг тканей опухоли образуется своеобразная капсула, и по мере роста ее размера, она просто раздвигает окружающие здоровые ткани.
Именно поэтому она и не оказывает особо неблагоприятного воздействия на организм (исключая опухоли головного мозга, способные сдавливать нервные центры в нем). В отличии от них, злокачественные опухоли ведут себя как настоящие захватчики. Они быстро растут и стремятся так или иначе распространиться по всему организму.
Злокачественные опухоли проникают в соседние ткани, разрастаются и разрушают их — это явление называется «инфильтративный рост», им свойственно рецидивировать — то есть вырастать снова после удаления, химиотерапии или лучевой терапии на том же самом месте, они способны вызывать слабость и истощение.
И, конечно, одна из ключевых их особенностей (во многом связанная с предыдущими) — это способность к метастазированию.
Внутренние захватчики
Метастазирование — это перенос опухолевых клеток за пределы «исторической родины» в различные органы и ткани. Там они образуют новые опухоли, называемые вторичными и близкие по структуре к первичной опухоли.
По мере увеличения числа клеток в новой «колонии», они начинают выделять вещества, стимулирующие образование и развитие вокруг нее сети сосудов и капилляров — это дает опухоли возможность «питаться», а так как за счет чрезвычайно быстрого роста питания ей также требуется больше, чем другим тканям, у больных раком может наблюдаться истощение — питательные вещества проходят мимо всего остального организма.
К несчастью, у раковых клеток довольно много разнообразных способов перемещаться по телу человека. Они могут проникать в лимфатические сосуды организма, добираясь сначала до ближайших лимфатических узлов, а уже оттуда мигрируя дальше и добираясь до других органов и тканей.
Раковые клетки перемещаются по кровеносным сосудам — при наличии злокачественной опухоли они все время присутствуют в крови, но большую их часть выслеживает и убивает иммунная система. Однако те, которые остаются незамеченными, добраются до других органов и тканей и образуют там новую опухоль.
Иногда, впрочем, раковые клетки считают дальние путешествия излишними и образуют новую опухоль прямо рядом со старой.
Направления для путешествий зависят в первую очередь от типа рака — рак легкого, например, дает метастазы в головной мозг, кости и надпочечники, а при раке почки образуются внутрисосудистые опухоли и опухоли костей. Раньше и обширнее метастазы наблюдаются у молодых людей, кроме того, метастазирование учащается с ростом опухоли. В среднем, как правило, метастазы появляются через 1-2 года после начала развития рака.
Метастазы, как и основная опухоль, значительно нарушают работу организма — они выделяют токсины и биологически активные вещества, вмешивающиеся в системы регуляции органов и тканей, разрушают здоровую ткань вокруг них, распадаются, умирая, и также отравляют организм. Химиотерапия и лучевая терапия проводятся в том числе для того, чтобы предотвратить появление метастазов. Но в случае, если они все-таки появляются — смерть онкологических пациентов как правило происходит именно из-за них.
Источник: https://theoryandpractice.ru/posts/7364-chto-takoe-metastazy-i-pochemu-kletki-opukholi-bessmertny