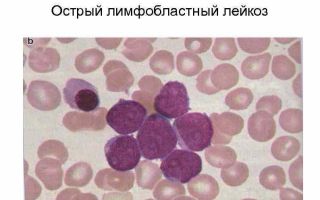
Гострий мієлоїдний лейкоз
Основним методом лікування гострого мієлоїдного лейкозу є хіміотерапія. Водночас таке лікування може сприяти розвитку рецидиву хвороби в майбутньому.
Що це таке
Лейкоз (рак крові) – захворювання кісткового мозку, при якому виробляється надмірна кількість незрілих аномальних клітин-попередників лейкоцитів. Ці клітини, накопичуючись в кістковому мозку, заважають діяльності нормальних клітин крові, що і призводить до основних проявів захворювання.
Різні клітини крові мають свою ієрархію розвитку: від клітин-попередників до зрілих клітин, що виконують усі свої функції. Лінія кровотворення, відповідальна за вироблення лімфоцитів називається лімфоїдною. Решта клітин крові відносяться до мієлоїдної лінії.
Гострий мієлоїдний лейкоз (ГМЛ) – злоякісна пухлина, при якій відбувається стрімке розмноження змінених білих кров’яних клітин.
Гострий мієлоїдний лейкоз вважається рідкісним захворюванням. Згідно зі статистичними даними (США) на його частку припадає 1,2% смертельних випадків від усіх злоякісних захворювань в США. Водночас ГМЛ є найпоширенішим видом гострого лейкозу серед дорослого населення.
Вірогідність розвитку гострого мієлоїдного лейкозу збільшується з віком.
Причини
Точні причини розвитку гострого мієлоїдного лейкозу досі не визначені. Разом з тим, існує ряд факторів, здатних привести до реалізації даного захворювання. До них відносяться:
- стан пре-лейкозу (мієлодиспластичний або мієлопроліферативний синдром);
- дія хімічних речовин. Існують дані про те, що препарати, які застосовуються при хіміотерапії, (зокрема, алкілуючі речовини) здатні збільшити ймовірність розвитку ГМЛ надалі. Згідно з медичними даними, найбільша ймовірність розвитку хвороби приходить на 3-5 роки після хіміотерапевтичного лікування. Небезпеку також можуть представляти хіміопрепарати на основі епіподофілотоксинів і антрациклінів. Спірним залишається питання про бензол, як чинник розвитку гострого мієлоїдного лейкозу;
- іонізуюче випромінювання підвищує ймовірність розвитку ГМЛ. Так, згідно зі статистичними даними, серед осіб, які пережили атомне бомбардування в Хіросімі і Нагасакі, рівень захворюваності ГМЛ вище;
- спадковість. Цей фактор не можна виключати, хоча б тому, що існують дані про сімейні випадки ГМЛ, захворюваність якого перевищує середньостатистичний. Більш достовірних даних, що вказують на можливі генетичні дефекти, поки ще немає.
Симптоматика
У клінічній картині гострого мієлоїдного лейкозу виділяють прояви наступних синдромів:
- Анемічний, для якого характерне зниження рівня гемоглобіну та еритроцитів. Проявляється анемічний синдром слабкістю, сонливістю, зниженням працездатності, серцевою недостатністю, гіпотензією, задишкою, блідістю шкірних покривів, стенокардією, кульгавістю і бронхо-легеневими захворюваннями.
- Гранулоцитопенічний, при якому знижується число гранулоцитів в крові. Для даного стану характерні інфекційні ускладнення (локальні чи генералізовані інфекційні процеси), висока температура, інтоксикація.
- Геморагічний, що виявляється крововиливами в шкірі, слизових оболонках, а також кровотечами у внутрішніх органах.
- Проліферативний – характеризується лімфаденопатіями, спленомегалією (збільшенням селезінки), збільшенням печінки, болями в кістках, головним болем, порушенням діяльності черепно-мозкових нервів та іншої симптоматикою неврологічного характеру.
- Інтоксикаційний синдром, який виявляється слабкістю, погіршенням апетиту, пітливістю і схудненням.
Лікування
Основним методом лікування гострого мієлоїдного лейкозу є хіміотерапія, спрямована на досягнення якнайшвидшої ремісії.
У більшості випадків хіміотерапевтична дія проводиться з використанням препаратів цитарабіну і ліків атрациклінового ряду.
Якщо в результаті індукційної терапії виявляється, що в кістковому мозку залишається не більше 5% бластних клітин, і у пацієнта не відзначається інших проявів захворювання, то в такому випадку констатується досягнення ремісії.
У 50-85% хворих з гострим мієлоїдним лейкозом відзначається хороший ефект від проведеного лікування. Приблизно у 20-40% хворих і через 5 років після лікування може не бути ніяких ознак захворювання. При трансплантації кісткового мозку ймовірність успішного лікування збільшується на 40-50%.
ЧИТАЙТЕ ТАКОЖ:
ЛЕЙКЕМІЯ (ЛЕЙКОЗ)
ЩО ТАКЕ РАК?
МЕТАСТАЗИ ПРИ РАКУ
Источник: https://ukrhealth.net/gostrij-miyeloidnij-lejkoz5655/
Гострий лейкоз крові
Гострий лейкоз не без підстав прирівнюють до злоякісних утворень. Дійсно, хвороба викликана надзвичайним розростанням молодих (бластних) клітин крові. Але, на відміну від пухлинних, вони не є атиповими за будовою або чужорідними для організму. Це «рідні» клітини, які раптом починають синтезуватися в великій кількості.
Залежно від морфології початкових елементів розрізняють 2 види гострих лейкозів: лімфобластний і мієлобластний.
Медична статистика встановила:
— загальна захворюваність становить 35 випадків на млн. населення;
— найбільш вразливі вікові періоди захворювання: дитинство і у дорослих старше 40 років;
— жінки і чоловіки хворіють з різною частотою, поширеність серед жінок — 7,7 на 100 тис.
, серед чоловіків — 13,2;
— співвідношення між лімфобластний і нелімфобластнимі формами змінюється в залежності від вікових груп, серед дітей — до 15 років лімфобластних більше в 4 рази (4: 1), а серед людей старше 35 років мієлобластні виявляються в 8 разів частіше (1: 8).
Причини лейкозу крові до теперішнього часу не виявлено. Більшість вчених вважають головною — зміни на рівні будови і складу хромосом.
Як розвивається хвороба
Зайві бластні клітини розростаються і займають місце нормальних елементів крові, витісняючи їх і пригнічуючи правильне кровотворення.
Під впливом лікування цитостатиками відбувається пристосування і прогресуючий зростання нових клональних клітин, у тому числі далі розвиваються бласти.
Метастази бластів виникають в селезінці, лімфовузлах, печінці (органах, які беруть участь в кровотворенні,) та інших частинах тіла (головний мозок, шкіра, легені, яєчка).
класифікації
Тривалий час вчені різних країн і клініцисти користувалися класифікацією (FAB), заснованої на «зовнішній вигляд» основних клітин: розміри, співвідношення між масою ядра і цитоплазми, будова і форма ядра. Доводи проти цього виду обліку пред’являли практичні гематологи, які займалися діагностикою та лікуванням.
Тому Всесвітня організація охорони здоров’я в 2001 році прийняла нову більш зручну класифікацію. До назв форми захворювання додається код пошкодженого хромосомного набору, зрозумілий для вчених-генетиків.
Види гострих лімфобластний лейкозів
Сучасна класифікація гострих лейкозів лімфобластного типу будується на визначенні маркерів імунних клітин (специфічних антигенів до певних клонам):
— якщо на поверхні клітин виявляються маркери до Т-лімфоцитів, Т-гострий лімфобластний лейкоз; — при спорідненість до В-ряду лімфопоезу — По-лімфобластний;
— загальна або змішана форма захворювання.
У групах виділені підвиди, що залежать від стадій розвитку (диференціації) клітин:
— пре-Т, про-Т, Т зрілий;
— пре-В, пре-пре-В, про-В.
Окремо виділені види, що супроводжуються відомими хромосомними аномаліями:
— з Філадельфійської хромосомою;
— з транслокаціями (заміною) однієї хромосоми на іншу і утворенням нового гена.
Види гострих нелімфобластних лейкозів
Форми нелімфобластних лейкозів з генетичними аномаліями теж враховують відому заміну місцями пронумерованих хромосом. Подібних класів виділено 4. Крім того, є підвиди:
— зі змінами всіх рядів клітин (мультилинейной дисплазією); — лейкоз на тлі іншого попереднього захворювання (прелейкемічною), що супроводжується розростанням або зміною структури клітин нелімфатіческого ряду; — захворювання без доведеного прелейкемічною періоду, але при виявленому порушенні будови більше половини клітинного складу за різними формами диференціювання;
— вторинний гострий лейкоз, що з’явився на тлі лікування онкологічного захворювання методом хіміотерапії.
До дуже рідкісним підвидів відносяться виділяються в дитячому віці:
— базофильная форма лейкозу, — гострий панміелоз і мієлофіброз,
— саркома миелоидного характеру.
Стара (морфологічна) класифікація
Якщо за морфологічними характеристиками форма лейкозу не входить в класифікацію ВООЗ, то в діагностиці користуються старими назвами і видами.
Франко-американо-британський різновид (FAB) пропонує облік гострих нелімфобластних лейкозів по аналізах крові і клітин кісткового мозку. Діагностика форми грунтується на кількості клітин, процентному складі. Для стислості кожним видом присвоєно буквене зображення з порядковим номером (М1, М2).
М1 — гострий мієлоїдний лейкоз (мієлобластний):
— в костномозговом речовині бластних кліток не менше 90% складу;
— інші 10% припадають на дозрівають гранулоцити (від промиелоцитов до сегментоядерних лейкоцитів).
М2 — різновид М1, але клітини характеризуються як «частково дозрілі»:
— бластних клітин від 30 до 90%;
— менше 20% клітин моноцитарного паростка;
— гранулоцитів — 10% і більше.
М3 — гострий лейкоз проміелоцітарний діагностується при виявленні у вмісті кісткового мозку промієлоцитарному клітин без додаткових тестів.
М4 — гострий лейкоз міеломонобластний:
— в кістковому мозку міститься від 30 до 80% клітин мієлоїдного паростка;
— в периферичної крові моноцитів і їх попередників 5х10 9 і більше в літрі.
Крім структури клітин, використовують реакцію забарвлення бластних клітин з α-нафтілестераза (позитивний і негативний варіанти).
При одночасному вмісті в крові еозинофілів не менше 5% форма захворювання називається М4е.
М5 — гострий монобластний лейкоз: монобласти в пунктаті становлять не менше 80%.
М7 — гострий мегакаріобластний лейкоз: в діагностиці необхідно иммунофенотипирование або електронна мікроскопія.
М0 — гостра рання мієлобластна форма: всі забарвлення дають негативний результат, для діагностики необхідно вивчення імунного типу клітин.
Клінічні прояви
Гострий лейкоз проявляється клінічними симптомами, незалежно від виду захворювання. Початок хвороби може бути раптовим або розвиватися поступово.
Порушена робота кісткового мозку викликає клінічні синдроми:
— анемічний — у пацієнта спостерігається блідість шкіри, скарги на загальну слабкість, сонливість, серцебиття;
— геморагічний — на шкірі мимовільно з’являються синці в місцях здавлення, тертя, ін’єкцій, дрібні точкові крововиливи (петехії), пацієнт страждає від носових кровотеч, у дівчат і жінок можливі рясні менструації, в важких випадках виникають прояви шлункового і кишкового кровотечі, крововиливи в мозок;
— розвиток імунодефіциту сприяє швидкому зараженню якими інфекціями (вірусні, бактеріальні), особливо важко вони протікають, якщо приєднується грибкова флора, у пацієнтів виявляють стоматити, герпетичні висипання, ангіни, у важких випадках запалення легенів, сепсис;
— синдром дисемінованого внутрішньосудинного згортання (ДВС), зазвичай викликає гострий лейкоз проміелоцітарний, згортання крові проходить стадії підвищення і різкого зниження, посилюються кровотечі.
специфічні ознаки
Гострий лейкоз має ряд специфічних ознак:
— Прояви загальної інтоксикації — підвищення температури, посилення пітливості, зниження апетиту, схуднення, слабкість.
— Болі в кістках хребта, великих трубчастих.
— Збільшення лімфовузлів в будь-якій зоні, вузли при пальпації щільні, круглі, еластичні, можуть бути груповими, спаяні між собою, хворобливі.
— Локалізація збільшених вузлів в області брижі викликає болі в животі. Якщо збільшуються загрудінні лімфовузли, то можливо здавлення бронха, стравоходу.
Відповідно, з’являється порушення дихання, ковтання.
— Поразка головного мозку (нейролейкемія) — частіше спостерігається при лімфобластній формі, симптоми пов’язані з метастазами клітинних розростань в оболонки і речовина головного і спинного мозку, спостерігаються головні болі, запаморочення, погіршення зору, зміна мови, координації рухів. — Лейкеміди (вузлики) на шкірі частіше дає гострий мієлоїдний лейкоз, міеломонобластний форма.
— Значне збільшення вилочкової залози (тимуса) сприяє здавлення органів середостіння.
— Поразка яєчок проявляється в асиметричному збільшенні, відсутності болів.
діагностика
Перші зміни після клінічних симптомів відзначають в аналізі крові. Будь-які різкі відхилення у формулі при нормальному, зниженому або підвищеному загальній кількості лейкоцитів викликають підозри на лейкоз.
Диференціація гострої або хронічної форм залежить від наявності молодих клітин на тлі відсутності проміжних (лейкемічний провал). Майже завжди є лімфоцитоз, тромбоцитопенія, анемія.
Основа діагностики — цитологічна характеристика пунктата кісткового мозку, визначаються характерні описані ознаки в миелограмме.
Цитохимический метод заснований на виявленні типових для різних бластних форм ферментів.
Методика іммунофенотіпірованія дозволяє типировать бластні клітини за характерними маркерами. Вона необхідна у випадках утруднення відмінності лімфобластного і мієлобластний лейкозу. Це важливо, оскільки потрібна різна лікування.
Генетичні дослідження клітин крові дозволяють встановити патологію хромосом, конкретну генетичну аномалію.
Аналіз спинномозкової рідини після пункції має значення в діагностиці ступеня ураження мозку.
На рентгенівському знімку грудної клітки можна побачити збільшені групи лімфовузлів в легких, середостінні.
Перед застосуванням хіміотерапії лікаря необхідні вихідні показники роботи печінки і нирок (біохімія крові), електрокардіограма, УЗД печінки, селезінки. За ним буде оцінюватися токсичний ефект лікування.
лікування
Лікування гострого лейкозу проводиться в спеціалізованих відділеннях. Починати його слід негайно. Головна мета терапії — досягнення тривалої ремісії хвороби, коли пацієнт не відчуває симптомів, стабілізується картина крові.
Сучасні методи терапії включають:
— хіміотерапію,
— біологічний спосіб,
— променевої метод,
— пересадку стовбурових клітин кісткового мозку донора, — видалення селезінки за показаннями (в пізніх стадіях).
— хіміотерапія
Метод хіміотерапії передбачає використання сильних лікарських засобів, здатних зруйнувати змінені клітини. Препарати вводяться внутрішньовенно, в спинномозковий канал.
Застосовується курсова терапія з розрахунком загальної дози препаратів на вагу хворого. Підбір препаратів і стандартного курсу визначається за ступенем порушення кровотворення.
Після стаціонарного лікування хворому призначають підтримуючу дозу для прийому на дому.
біометод
До біологічного методу відносять стимуляцію власного імунітету організму для гальмування росту ракових клітин. З цією метою використовують моноклональні антитіла, Інтерферон.
променева дія
Променева терапія — вплив радіацією на кістковий мозок хворого. Лікарі встановлюють місце для опромінення, разову і курсову дозу. Часто використовується перед пересадкою кісткового мозку.
Трансплантація кісткового мозку
Пересадка здорових стовбурових клітин кісткового мозку дозволяє підвищити дозу хіміопрепаратів і променевої терапії. З пересаджених клітин розвиваються нормальні лейкоцити.
Небажані ефекти лікування
Перераховані методики не обходяться без ускладнень. Важливо, що вони очікувані і знайомі лікарям. Пацієнтам теж розповідають про негативні наслідки терапії.
При хіміотерапії наступає: кровоточивість, посилюється слабкість через недокрів’я, облисіння. На губах з’являються виразки, уражається слизова кишечника (нудота, втрата апетиту, блювота).
Після біологічних методик можлива поява висипу на шкірі, свербіння, гриппоподобного стану з високою температурою.
При курсі радіаційної терапії пацієнт відчуває підвищення слабкості, шкіра сохне, старіє, червоніє.
Трансплантація не завжди буває успішною: якщо розвивається реакція відторгнення, виникає безпосередня загроза для всіх внутрішніх органів, особливо для печінки.
підтримуюча терапія
У стані ремісії лікування пацієнта не припиняється, йому показана підтримуюча терапія і симптоматичні засоби для профілактики рецидивів хвороби. Використовуються антибактеріальні препарати, переливання крові, вітаміни. Всі кошти призначаються тільки лікарем.
прогноз
Прогноз визначається за показником п’ятирічної виживаності пацієнтів. При гострий лімфобластний лейкоз він в даний час досяг 68,8% у дорослих, при миелобластном — 24,9%.
При лікуванні гострого лейкозу показники у дітей значно краще: 85% у випадках гострого лімфобластного захворювання, від 60 і 70% — при мієлобластній формі.
Вважається, що можна говорити про клінічному одужанні дітей, які перенесли гостру форму лейкозу.
Найбільш несприятливими формами поки є: гострий лімфолейкоз з Філадельфійської хромосомою, нелімфобластні форми з множинною дисплазією клітин.
Описані варіанти — М2, М3 і М4 — відрізняються хорошою реакцією на хіміотерапію.
Успіхи в лікуванні дитячого лейкозу дозволяють сподіватися на отримання нових засобів і досягнення тривалої ремісії при захворюваннях дорослих.
ActionTeaser.ru – тизерная реклама
► ► ►
Источник: http://medix.in.ua/nedug/cardio/hostryi_leikoz_krovi/
Гострий мієлоїдний лейкоз
Лейкоз . або лейкемія — захворювання кісткового мозку. в побуті іноді зване «раком крові». При лейкозі порушено нормальне кровотворення.
виробляється надмірна кількість аномальних незрілих клітин крові, зазвичай попередників лейкоцитів. Ці бластні клітини.
розмножуючись і накопичуючись в кістковому мозку, заважають виробленню і функціонуванню нормальних клітин крові, що й обумовлює основні симптоми захворювання.
Як відомо, різні клітини крові розвиваються по-різному і мають різних попередників — тобто відносяться до різних лініях кровотворення (див. Схему в статті «Кровотворення»). Лінія кровотворення, яка веде до появи лімфоцитів.
називається лімфоїдної ; інші ж лейкоцити і інші клітини крові відносяться до мієлоїдній лінії.
Відповідно, розрізняють лейкози з клітин-попередників лімфоцитів (такі лейкози називають лімфобластний, лімфоцитарними або просто лімфолейкоз) і з попередників інших клітин (такі лейкози називають мієлобластний, мієлоїдний або просто мієлолейкоз).
Гострий мієлоїдний лейкоз (ГМЛ, гострий мієлобластний лейкоз, гострий мієлолейкоз, гострий нелімфобластний лейкоз) — захворювання, порівняно рідко зустрічається у дітей, проте з віком частота його зростає.
Термін «гострий» означає швидкий розвиток хвороби, на противагу хронічного лейкозу. Термін «мієлоїдний» означає, як зазначено вище, що незрілі клітини, які складають основу хвороби, належать до так званої мієлоїдною лінії кровотворення.
Ці клітини — як правило, мієлобласти і їх нащадки, але можливо також присутність інших видів бластних клітин.
У рамках франко-американсько-британської морфологічної класифікації (ФАБ, FAB) виділяють 8 основних варіантів ГМЛ.
Деякі дуже рідкісні різновиди ГМЛ не включені в цей список. Варіанти ГМЛ з М3 по М7, що мають власні назви і деякі специфічні особливості, більш детально розглянуті в окремих розділах нашого довідника.
Частота народження, фактори ризику
ГМЛ складає у дітей близько 15% всіх випадків онкологічних захворювань кровотворної системи, тобто зустрічається у них помітно рідше, ніж гострий лімфобластний лейкоз. Серед дітей до 14 років частота ГМЛ складає приблизно 0.6-0.
8 випадків на 100 тисяч осіб на рік, однак у віці після 40-45 років відбувається різкий підйом захворюваності. Більшість хворих ГМЛ — літні люди.
На відміну від гострого лімфобластного лейкозу, найбільш характерного для дитячого віку, при ГМЛ діти складають всього 10% хворих.
У більшості випадків ГМЛ неможливо назвати безпосередню причину захворювання. Однак деякі фактори підвищують ймовірність виникнення ГМЛ: вплив ряду хімічних препаратів, іонізуючої радіації (в тому числі в ході попереднього лікування інших онкозахворювань), іноді — випадки захворювання ГМЛ серед найближчих родичів, що говорить про певну роль генетичної схильності.
Розвитку ГМЛ можуть передувати деякі захворювання кровотворної системи, такі як мієлодиспластичний синдром. Нарешті, ризик ГМЛ підвищений при певних генетично обумовлених аномаліях, включаючи синдром Дауна, анемію Фанконі і деякі інші стани.
Ознаки та симптоми
ГМЛ характеризується безліччю різних ознак і у різних хворих може виявлятися по-різному. Ведучими, як правило, є ознаки анемії. стомлюваність, блідість, задишка, зниження апетиту. Недолік тромбоцитів проявляється підвищеною кровоточивістю при порізах і ударах, носовими кровотечами, «безпричинним» появою синців і синців.
Нерідко зустрічаються стійкі до лікування інфекції, так як у хворого для боротьби з ними надто мало «нормальних» (зрілих, функціональних) лейкоцитів. Може виникнути ураження слизових оболонок рота і шлунково-кишкового тракту, припухлість ясен. Нерідко підвищена температура тіла, зустрічаються болі в кістках.
Іноді виникають пухлини з лейкемических клітин поза кістковим мозком — міелосаркома (хлорома) .
Так як більшість симптомів може бути пов’язані і з іншими захворюваннями і не специфічно для ГМЛ, перед початком лікування необхідно уточнення діагнозу на підставі лабораторних методів, яке в терміновому порядку проводиться в лікарняних умовах.
Діагностика
При ГМЛ виникають зміни в звичайному клінічному аналізі крові. недолік еритроцитів і тромбоцитів. найчастіше надлишок лейкоцитів. причому багато хто з них представлені незрілими формами.
Але надійно поставити діагноз можна тільки при дослідженні зразка кісткового мозку.
Відповідно до критеріїв Всесвітньої організації охорони здоров’я, діагноз ГМЛ ставиться, якщо зміст мієлобластів в кістковому мозку не менше 20% (згідно з франко-американо-британської классіфіціі FAB, граничним значенням є 30%).
Для лікування і оцінки прогнозу захворювання важливо не тільки підтвердити діагноз «лейкоз», а й розрізняти гострий лімфобластний лейкоз і ГМЛ, розмежовувати лейкоз і мієлодиспластичний синдром. а також визначати конкретний варіант ГМЛ (див. вище).
Для цієї мети застосовується не тільки морфологічне дослідження клітин (мікроскопічне дослідження спеціальним чином забарвлених препаратів), а й цитохимический аналіз, а також иммунофенотипирование (вивчення білків-антигенів на поверхні клітин).
Цитогенетичні дослідження застосовуються для виявлення хромосомних перебудов — так званих транслокаций. мають велике значення для визначення варіанту хвороби і прогнозу.
Точна діагностика ГМЛ і його варіантів іноді являє собою складну задачу, що вимагає участі висококваліфікованих гематологів і гемопатологов в діагностичному процесі.
Як і при гострому лімфобластний лейкоз. результати діагностичних досліджень при ГМЛ використовуються для віднесення пацієнта до тієї чи іншої групі ризику . Це необхідно для того, щоб визначити тактику лікування, оцінити як імовірність відповіді на хіміотерапію.
так і ризик подальшого рецидиву. У пацієнтів, що належить до групи низького ризику, більше шансів досягти довгострокової ремісії при стандартному хіміотерапевтичному лікуванні, а при високому ризику для успіху терапії може знадобитися трансплантація кісткового мозку.
Групу ризику визначають багато чинників. Перерахуємо деякі з них:
- Вік: у хворих середнього та похилого віку прогноз в середньому гірше, ніж у дітей і молодих людей.
- Хромосомні зміни в лейкемических клітинах. Так, транслокації t (15; 17) або t (8; 21) визначають у хворих нижчий ризик. У той же час, наприклад, певні зміни хромосом 5 і 7 пов’язані з погіршенням прогнозу.
- Варіант лейкозу. Деякі варіанти ГМЛ (такі як М0, М6, М7) пов’язані з високим ризиком, а деякі, навпаки, порівняно добре піддаються сучасної терапії (ГМЛ М3).
- З більш високим ризиком пов’язаний вторинний лейкоз, що виник на тлі іншого гематологічного захворювання — такого як мієлодиспластичний синдром або анемія Фанконі. — Або після проходження лікування (хіміотерапія, опромінення) з приводу будь-якої злоякісної пухлини. Ризик також різко підвищується при рецидив лейкозу.
Головним методом лікування ГМЛ є хіміотерапія. Як у випадку гострого лімфобластного лейкозу. лікування включає фази індукції ремісії і консолідації; іноді застосовується також підтримуюча терапія.
Індукція ремісії — інтенсивна терапія, спрямована на досягнення ремісії лейкозу.
При більшості варіантів ГМЛ індукція ремісії проводиться за допомогою інтенсивної хіміотерапії з використанням цитарабіну (цітозара) і ліків антрациклінового ряду (даунорубіцин, ідарубіцин), іноді з додаванням інших препаратів — наприклад, етопозиду або мітоксантрону. Стандартом є курси «7 + 3», при яких хворому протягом 7 днів вводять цитарабін, причому протягом трьох днів — у поєднанні з антрациклінових препаратом.
Специфічною особливістю терапії при гострому промієлоцитарному лейкозі (ГМЛ М3) є використання ліки ATRA (повністю транс-ретиноєва кислота, третиноин).
Якщо в результаті терапії індукції виявляється, що в кістковому мозку стало менше 5% бластних клітин і у пацієнта немає інших проявів хвороби (в тому числі ознак нейролейкеміі), то констатується досягнення ремісії.
В результаті курсів індукції вдається досягти ремісії у переважної більшості пацієнтів. Однак досягнута ремісія не може бути стійкою без терапії консолідації . тобто закріплення ремісії.
У фазі консолідації знищуються залишкові кількості аномальних бластних клітин, щоб уникнути рецидиву захворювання.
Найважливішим препаратом в фазі консолідації при лікуванні ГМЛ є цитарабін, часто в високих дозах; в різних поєднаннях використовуються також даунорубіцин, 6-меркаптопурин, ифосфамид, мітоксантрон, етопозид і ін.
На етапах індукції та консолідації внутрішньовенне введення хіміотерапевтичних препаратів проводиться в умовах лікарняного стаціонару.
Підтримуюча терапія використовується далеко не в усіх випадках (на відміну від гострого лімфобластного лейкозу), однак при варіанті ГМЛ М3 вона важлива. Ця терапія менш інтенсивна, ніж терапія індукції та консолідації, і не вимагає перебування в лікарні.
Нейролейкемія менш характерна для ГМЛ, ніж для гострого лімфобластного лейкозу. Найчастіше вона зустрічається при варіантах ГМЛ М3, М4 і М5. Для її лікування та профілактики можуть використовуватися цитарабін, метотрексат і глюкокортикоїди. вводяться інтратекально .
за допомогою люмбальної пункції спинномозкового каналу. Зрідка може використовуватися також опромінення голови (краніальніше опромінення).
У дітей ризик поширення лейкозу в центральну нервову систему вище, ніж у дорослих, тому профілактична хіміотерапія для його запобігання використовується частіше.
Для зниження ймовірності рецидиву пацієнтам з групи високого ризику може бути показана трансплантація кісткового мозку. Показаннями до трансплантації можуть служити, наприклад,
- транслокации і інші цитогенетичні зміни в лейкемических клітинах, пов’язані з високим ризиком,
- рецидив лейкозу,
- розвиток ГМЛ на тлі мієлодиспластичного синдрому або іншої хвороби крові, а також після попереднього лікування злоякісних пухлин.
Імовірність успіху трансплантації максимальна, якщо проводити її після досягнення першої ремісії. У дітей трансплантації виробляються частіше, ніж у дорослих, і в середньому більш успішні.
В ході інтенсивної хіміотерапії ГМЛ практично завжди в тій чи іншій мірі пригнічується нормальне кровотворення. Тому багатьом хворим ГМЛ необхідні переливання компонентів крові. тромбоцитів, щоб уникнути кровотеч і еритроцитів для лікування анемії. Переливання донорських лейкоцитів (гранулоцитів) потрібні тільки у випадках важких інфекційних ускладнень.
Оскільки і лейкоз сам по собі, і використовувана при його лікуванні хіміотерапія різко знижують опірність організму до різних інфекцій, то хворим під час лікування часто необхідні ефективні антибактеріальні, протигрибкові та противірусні ліки для профілактики і терапії інфекційних ускладнень. Небезпеку становлять як звичайні, так і опортуністичні інфекції. Зокрема, серйозну проблему представляють такі грибкові інфекції, як кандидоз та аспергільоз.
Лікування ГМЛ накладає обмеження на спосіб життя хворого. В ході інтенсивної хіміотерапії необхідно дотримуватися дієти і строгі правила гігієни, а також мінімізувати контакти з зовнішнім світом, щоб уникнути інфекцій. Лікарі та медсестри повідомляють кожному хворому, що йому можна і що не можна на поточному етапі лікування.
Загальна тривалість лікування при різних формах ГМЛ складає від декількох місяців до 2-3 років.
Прогноз
Без лікування ГМЛ, як правило, призводить до загибелі хворого протягом декількох місяців, іноді навіть кількох тижнів. Однак при сучасному лікуванні багатьох можна врятувати. Прогноз залежить від конкретної різновиди миелолейкоза, цитогенетичних особливостей (тобто хромосомної структури лейкемических клітин), віку, загального стану хворого і інших чинників.
В даний час близько 50-60% дітей, хворих ГМЛ, одужують. У середньому і літньому віці, на жаль, результати гірше.
Слід зазначити, що більшість пацієнтів з ГМЛ — це саме літні хворі. У порівнянні з молодими вони важче переносять лікування і гірше на нього відповідають.
Всього у 5-15% пацієнтів старше 60 років вдається досягти тривалої ремісії.
Для інших найчастіше основним стає підтримуючу терапію (боротьба з інфекціями, переливання компонентів крові, знеболювання) для деякого продовження життя і поліпшення її якості.
Підписатися на розсилку
Источник: http://medmed.in.ua/gostrij-miyelojidnij-lejkoz/
Мієлоїдний лейкоз
Зміст:
- Як виглядає збій кровотворення?
- Причини
- Види миелоцитарного лейкозу
- Клініка гострого мієлоїдного лейкозу
- Клініка хронічного мієлолейкозу
- Як проводиться діагностика?
- Лікування
- Ускладнення від терапії
- Можна прогнозувати результат хвороби?
Мієлоїдний лейкоз (мієлобластний, миелоцитарный, мієлолейкоз) входить в групу онкологічних захворювань крові, оскільки викликаний зміною шляху кровотворення і надмірним розростанням клітин мієлобластного паростка кісткового мозку.
Стрімке розмноження функціонально неповноцінних клітин призводить до порушення переносу кисню, падіння імунітету та інших патологічних зрушень. Ступінь ураження визначається часткою нормальних еритроцитів, тромбоцитів, лейкоцитів.
Хвороба до цього часу вважається невиліковною. Позитивним результатом лікування прийнято називати тривалу ремісію і п’ятирічну виживаність пацієнтів.
Як виглядає збій кровотворення?
В нормальних умовах кістковий мозок є «базою», де виробляються елементи крові. Процес починається з перетворення стовбурових клітин в бластні. У ньому беруть участь всі трубчасті і плоскі кістки скелета.
Встановлено цікава властивість: при трансплантації кісткового мозку стовбурові клітини самі «знають», де потрібно влаштуватися. Показано, що близько 85% направляються в кістковий мозок, хоча його масова частка становить лише 6% ваги тіла. А інші розподіляються між легкими, селезінкою і печінкою.
Цю реакцію назвали «хоумингом», ймовірно вона пов’язана з передаванням інформації між клітинами по своїх каналах.
В кістковому мозку продукуються попередники всіх клітин крові, але відбувається «дозрівання» тільки еритроцитів, тромбоцитів і деяких видів лейкоцитів. Для остаточного дозрівання лімфоцити переходять в селезінку і вилочкової залози.
Загальна диференціація йде по 12-ти напрямках (поки вивченим). Керує нею генний механізм.
Встановлено поєднання генів, що сприяють розвитку правильних клонів клітин крові і викликають збій системи поділу на різному рівні з утворенням «недозрілих» примірників.
Крім того, частота поділу бластних клітин пов’язана з концентрацією в крові особливих речовин (поэтинов). Вони специфічні для кожного напряму (еритропоетин, тромбопоэтин). В результаті бластні (наймолодші) клітини замінюються дозріваючими формами. Вони в назві відрізняються приставкою «про», наприклад, проміелоціти.
Збій остаточного дозрівання при мієлоїдному лейкозі наступає на будь-якому рівні. У результаті не тільки накопичуються непотрібні формені елементи крові, але і заносяться в інші органи і там починають прискорено ділитися.
Розростаючись, великі бластні клітини витісняють нормальні еритроцити, тромбоцити і лейкоцити
Причини
Причини патологічної мутації стовбурових клітин до теперішнього часу не встановлені. Вивчено вплив деяких факторів:
- спадковість, зв’язок з хромосомними комбінаціями, що доводиться більш частим виявленням хронічного мієлоїдного лейкозу у осіб з синдромом Дауна;
- залежність від вірусних захворювань;
- терапія цитостатичними препаратами з іншого приводу онкозахворювання;
- наслідок впливу проникаючої радіації при аваріях джерела, військових діях та променевої терапії;
- токсична дія вуглеводнів (бензолу), речовин, що належать до зброї масового знищення.
Виявлено зв’язок гострого промиелоцитарного лейкозу з перенесеним на рак молочної залози у жінок (виникає у 40% пацієнтів). Вражає людей 40-50 років.
Вивчення факторів впливу на кровотворення триває. Знаючи конкретний механізм «поломки», легше підібрати необхідне лікування.
Види миелоцитарного лейкозу
Розбіжності за видами та формами полягають у характері клінічного перебігу та переважній типі накопичених клітин.
За течією розрізняють:
- гостру форму;
- хронічний мієлоїдний лейкоз.
При хронічному перебігу не тільки спостерігається уповільнене розгортання симптомів хвороби, але і в крові визначається особливий зрушення, не характерний для гострої форми. Тому на відміну від соматичних захворювань перехід гострої форми в хронічну неможливий.
Гострий мієлолейкоз, згідно класифікації ВООЗ, підрозділяється на види залежно від виявленого впливу різних ділянок хромосом.
Інша діюча класифікація, затверджена гематологами США, Франції і Великобританії, враховує 9 підвидів за ступенем зрілості лейкоцитів. Виділення має сенс не тільки науковий, але й передбачає однакову оптимальну стандартну терапію. До них відносять по мірі дозрівання клітин:
- лейкоз без дозрівання;
- з дозріванням;
- з мінімальною диференціюванням клітинного складу.
По переважному складу клітинних форм:
- промиелоцитарный лейкоз;
- миеломоноцитарный — накопичення клітин-попередників моноцитів і гранулоцитів;
- миеломоноцитарный у поєднанні з еозинофілією;
- міеломонобластний лейкоз — монобласты становлять більшість клонів;
- мегакаріобластний;
- базофильный;
- група эритроидных лейкозів.
Хронічний миеломоноцитарный лейкоз теж являє собою кілька типів клітин-попередників:
- миелоцитарный лейкоз з філадельфійською хромосомою і без неї;
- ювенільний миеломоноцитарный лейкоз;
- нейтрофільний і еозинофільний види;
- первинний мієлофіброз.
Клініка гострого мієлоїдного лейкозу
Гострою формою мієлоїдного лейкозу хворіють як дорослі (частіше старше 40 років), так і діти. Поширення ракових клітин із заміною на лейкемічні види дуже агресивне, захворювання швидкоплинне. Без лікування людей гине через кілька місяців. Симптоми розвиваються відразу все. У пацієнта з’являються:
Радимо вам прочитати:Гострий мієлобластний лейкоз і його лікування
- кровотечі з носа;
- болі в кістках;
- загальна слабкість;
- виражена пітливість в нічний час;
- задишка без фізичного навантаження;
- схильність до частих інфекційних захворювань;
- втрата апетиту, зниження ваги тіла;
- тривала невисока температура тіла.
При огляді звертає на себе увагу:
- виражена блідість шкіри з дрібними петехиальными крововиливами;
- гематоми (синці, синці) на різних ділянках тіла;
- запалення ясен, стоматит;
- збільшення селезінки незначно, пальпація безболісна.
У кожного десятого пацієнта виявляються шкірні хлоромы (ущільнення з розрослися лейкемічних клітин).
Часто початок пов’язують з вірусною інфекцією (грип, ГРВІ). Дуже рідко хвороба протікає безсимптомно і виявляється з аналізу крові.
Клініка хронічного мієлолейкозу
На хронічну форму мієлолейкозу припадає 15% всіх випадків лейкозів. Вона зустрічається в будь-якому віці, частіше у літніх чоловіків. Виявлення філадельфійської хромосоми дозволило налагодити діагностику хвороби, зв’язати з більш важким прогнозом.
Протягом проходить 3 стадії і триває роками.
В хронічну стадію (3-4 роки) симптоматика може бути відсутнім. Її виявляють збільшення печінки і селезінки, наявності в аналізі периферичної крові промієлоцитів і бластних форм.
Проміжна стадія (акселерації) триває кілька місяців, характеризується:
- появою слабкості;
- підвищеною температурою тіла.
Ці симптоми проявляються на тлі наростання збільшення печінки і селезінки. Своєчасним лікуванням може бути затримана у часі.
Період бласттрансформації або бластного кризу (термінальний) дуже швидкоплинний, закінчується летально, незважаючи на лікування. В крові, кістковому мозку обсяг клонів досягає 25%. Дія цитостатиків у 10% випадків призводять до миелофиброзу (заміщення кісткового мозку клітинами-фібробластами).
Переливання крові в хронічну стадію допомагає заповнити запас нормальних клітин
Один з підвидів хронічних форм — ювенільний миеломоноцитарный лейкоз зустрічається у дітей 2-х – 4-х річного віку. Пов’язаний з хромосомними аномаліями.
Симптоми не мають відмінностей від гострої форми, але проявляються поступово:
- дитина млявий, апатичний;
- часто схильний до інфекційних захворювань;
- відмовляється від їжі;
- погано набирає вагу;
- відстає у розвитку;
- страждає частими носовими кровотечами.
Для типових симптомів хронічного мієлолейкозу характерні:
- болі в лівому підребер’ї в зв’язку з збільшенням селезінки, иррадиирующие в спину;
- болючість при пальпації печінки і селезінки;
- при підвищенні в базофілів периферичної крові до 30% у хворого з’являється свербіж шкіри, відчуття жару (викликані ростом концентрації гістаміну);
- болі в суглобах і значне підвищення температури вказують на наближення термінальній стадії.
При цьому велика вірогідність інфаркту селезінки, збільшуються лімфовузли, у зв’язку з поразкою центрів головного мозку проявляються парези і паралічі.
Як проводиться діагностика?
Щоб поставити правильний діагноз, необхідно правильно оцінити:
- розгорнутий аналіз крові (досвідчений лікар-лаборант вміє відрізняти клітини-попередники від нормальних, підрахунок лейкоцитарної формули виявить зростання бластів і недозрілих клонів);
- зменшення чисельності еритроцитів і тромбоцитів вказує на їх придушення бластними клітинами;
- біохімічні тести на білок, білірубін, ферменти підтверджують думку про порушення роботи печінки і селезінки;
- дослідження кісткового мозку стегнової кістки дозволяє не тільки з’ясувати напрямок переродження кровотворення, але і провести генетичний аналіз на філадельфійську хромосому.
З метою дослідження хромосомних аномалій застосовують спосіб полімеразної ланцюгової реакції, філадельфійська хромосома є специфічним маркером мієлоїдного лейкозу
Додатково можуть знадобитися:
- УЗД печінки та селезінки;
- магнітно-резонансна або комп’ютерна томографія для виключення тромбозу венозної системи внутрішніх органів.
Лікування
Тактика лікування залежить від стадії захворювання, в якій виявлений пацієнт. При безсимптомному перебігу і невеликих змінах призначається збалансоване харчування, вітаміни. Однак найбільш ефективним вважається застосування медикаментів цитостатичного напрямки впливу.
Серед мієлоїдних форм лейкозу максимальна чутливість до застосування транс-ретиноєвої кислоти (змінений вітамін А і триоксид миш’яку) спостерігається при гострому промиелоцитарном мієлолейкозі.
Цьому препарату вдається вплинути на генний фактор і змінити патологічну трансформацію клітин. При цьому, на відміну від цитостатиків, злоякісні клітини не вбиваються.
Подібний вид терапії називається індукованою.
Вінкристин — представник цитостатиків, призначається строго за показаннями
Із цитостатичних препаратів застосовують:
- Міелосан,
- Міелобромол,
- Алопуринол,
- Гидроксимочевина.
У термінальну стадію призначають:
- Цітозар,
- Рубоміцін,
- Вінкристин.
У гематології розроблені стандартні протоколи (схеми) лікування. Вони змінюються залежно від індивідуальної реакції пацієнта. Після досягнення ремісії потрібна підтримуюча терапія малими дозами препаратів. Категорично забороняється самостійно змінювати дозування і відмовлятися від завершення повного циклу лікування.
Курс променевої терапії використовується при збільшенні селезінки.
Порушення згортання доводиться компенсувати переливання свіжозамороженої еритроцитарної маси.
Трансплантація кісткового мозку від підібраного донора може призвести до тривалої ремісії.
Ускладнення від терапії
Застосування сильнодіючих цитостатиків загрожує розвитком ускладнень або побічних ефектів:
- у пацієнтів виникають прояви інтоксикації від дії препаратів (нудота, блювання);
- випадає волосся після променевої терапії;
- можливі зміни в шлунку і кишечнику від запалення до виразки слизової.
В процесі лікування можуть виникнути 2 стани, загрозливі для життя хворого.
ДВЗ-синдром
Пов’язаний з масивною загибеллю лейкозних клітин і надходженням в кровотік прокоагулянтов. Настає тромбування дрібних капілярів. Для зняття необхідне введення Гепарину, глюкокортикоїдів.
Люди, що оточують пацієнтів з лейкозом, повинні дотримувати строгу санітарну гігієну, оскільки хворі не мають захисту від інфекції
Ретиноидный синдром
Характеризується такими проявами:
- сильна лихоманка;
- випіт в плевральну або перикардіальну порожнини;
- виражена задишка;
- падіння артеріального тиску.
Летальність при прояві цих синдромів досягає 20%.
Можна прогнозувати результат хвороби?
Прогноз залежить від стадії захворювання, форми, реакції пацієнта на лікування. При гострих миелолейкозах вдається домогтися п’ятирічної виживаності для 15-70% пролікованих пацієнтів. Ремісія настає у 30-78% хворих.
При хронічній формі найбільш сприятливі результати досягаються, якщо призначити лікування в початковій стадії (майже 85%). При виявленні у стадії прогресування протягом найближчих двох років гине 10% пацієнтів, з третього року — по 15%.
Розроблено моделі прогнозування летального результату залежно від всієї сукупності несприятливих факторів. У них враховуються:
- вік;
- розміри селезінки;
- частка бластних клітин в крові;
- кількість тромбоцитів і базофілів.
Більшою надією на одужання відрізняються хронічні форми захворювання, ніж гострі. Тому так важливо починати термінове лікування, не затягувати діагностику, не піддавати сумніву рекомендації лікарів.
Наукові дослідження з кожним роком приносять нові досягнення в питаннях терапії. Необхідно налаштовувати пацієнта на досягнення ремісії і подальше спостереження.
Источник: http://jazdorov.com.ua/hvoroba/miyeloyidnyj-lejkoz.html
Гострий мієлоїдний лейкоз
Гострий мієлоїдний лейкоз (ГМЛ) – це рідкісний вид онкології, розвивається в будь-якому віці, але частіше зустрічається у людей старше 65 років.
Якщо Ви розглядаєте варіанти лікування гострого мієлоїдного лейкозу в Ізраїлі, ми допоможемо Вам у вирішенні цього завдання.
Наш центр «TheBestMedic», маючи досвід роботи на ринку послуг медичного туризму більше 10 років, може запропонувати організацію діагностики в Ізраїлі. Це комплексна послуга, яка передбачає підбір високопрофесійних експертів, профільного медичного центру, організацію та координування всіх видів обстежень, супровід, підбір та бронювання житла, транспортні послуги та багато іншого.
Записатися на консультацію
Про специфіку лікування в Ізраїлі можна дізнатися більше в статтях – « Медичний туризм в Ізраїлі або лікування без посередників », « Державні і приватні клініки Ізраїлю – переваги і недоліки для іноземних туристів».
Як правило, процес синтезу клітин крові є впорядкованим і контрольованим. При гострому мієлолейкозі він виходить з-під контролю, проводиться велика кількість аномальних клітин.
В основному це незрілі білі клітини крові, при деяких менш поширених типах ГМЛ – незрілі тромбоцити або еритроцити. Вони не функціонують належним чином.
Це призводить до підвищеного ризику інфекції, анемії і гематом у зв'язку з дефіцитом здорових еритроцитів і тромбоцитів.
Незрілі клітини заповнюють кістковий мозок, займаючи простір, необхідне для синтезу здорових клітин крові. Деякі лейкемические клітини проникають в кров і циркулюють по всьому тілу.
Причини гострого мієлоїдного лейкозу
Існує ряд факторів, які можуть збільшити ризик розвитку гострого мієлоїдного лейкозу. Розглянемо їх.
опромінення
Люди, які зазнали впливу високих рівнів радіації в результаті подій в ядерній промисловості, мають більш високу ймовірність розвитку гострого мієлолейкозу .
Куріння і вплив хімічних речовин
Багато хто знає, що куріння пов'язують із злоякісними хворобами легень, ротової порожнини, гортані, але не мають уявлення, як воно впливає на клітини, які не вступають в безпосередній контакт з димом. Канцерогенні речовини в димі поглинаються легкими і поширюються через кровотік по багатьом частинам тіла.
У складі сигаретного диму відзначається висока концентрація бензолу. У дуже рідкісних випадках хвороба розвивається в зв'язку з тривалим впливом цієї хімічної сполуки.
Бензол є розчинником, який використовується в гумовій, взуттєвій промисловості і в суміжних з бензином галузях, на нафтопереробних і хімічних заводах.
Він є в складі деяких клеїв, миючих засобів, фарб і художнього приладдя.
В Ізраїлі проводяться дослідження, спрямовані на вивчення ГМЛ, на розробку нових протоколів імунотерапії, на застосування точкової хіміотерапії, вакцинації злоякісними клітинами в лікуванні гострої лейкемії.
Замовити безкоштовний дзвінок
Деякі дослідження показують дію формальдегіду одним з факторів ризику ГМЛ.
лікування раку
Іноді хіміотерапія або променева терапія стають причиною розвитку гострого мієлоїдного лейкозу через кілька років. Імовірність збільшується, коли певні хіміопрепарати комбінують з опроміненням. Такий вид лейкемії називається вторинним.
Цитостатики під назвою алкілуючі агенти (циклофосфамід, прокарбазін, хлорамбуцил, мелфалан, бусульфан) і препарати платини (цисплатин і карбоплатин) пов'язують з підвищеним ризиком ГМЛ. А також інгібітори топоізомерази II (етопозид, Теніпозід, мітоксантрон, епірубіцин, доксорубіцин).
хвороби крові
Люди з певними захворюваннями крові, такими як мієлодисплазія або мієлопроліферативні патології (мієлофіброз, поліцитемія, есенціальна тромбоцитемія), мають підвищену ймовірність розвитку гострого мієлолейкозу.
генетичні порушення
Певні генетичні захворювання – синдром Дауна, первинний ізольований синдром Фанконі, синдром Блума, атаксія-телеангіектазії, синдром Лі-Фраумені, нейрофіброматоз 1 типу збільшують ризик гострого мієлоїдного лейкозу.
До невизначеним і спірним чинників відносять вплив електромагнітних полів (проживання поблизу ліній електропередач), а також вплив пестицидів і гербіцидів.
Найчастіше люди хворіють в літньому віці, в більшій мірі чоловіча частина населення. Наявність в сімейному анамнезі родича з ГМЛ збільшує ризик хвороби.
Симптоми гострого мієлоїдного лейкозу
Більшість ознак захворювання є наслідками дій лейкозних клітин в кістковому мозку, які роблять його нездатним продукувати здорові клітини.
Основні симптоми миелолейкоза:
- Блідість, втома і задишка через анемії, викликаної дефіцитом еритроцитів.
- Часті інфекції внаслідок нестачі здорових лейкоцитів.
- Низький рівень тромбоцитів викликає гематоми, рясні місячні у жінок, кровоточивість ясен, кровотечі з носа, точкові крововиливи на шкірі (петехії).
- Жар і пітливість внаслідок інфекції або лейкемії.
Інші, менш поширені симптоми миелолейкоза викликані скупченням лейкозних клітин в певній частині тіла. Болі в кістках можуть бути спровоковані тиском бластів в кістковому мозку. Зосередження їх під шкірою стає причиною формування блакитно-фіолетових областей, в яснах – набрякового стану.
Іноді буває, що ознак захворювання як таких не було, а хвороба була виявлена під час звичайного аналізу крові.
Ознаки гострого мієлоїдного лейкозу можуть з'явитися протягом декількох тижнів, але в основному люди хворіють досить швидко.
Достовірна і точна діагностика визначає ефективність лікування. Фахівці з лабораторних досліджень в клініках Ізраїлю володіють великим досвідом і високим рівнем знань. Крім того, важливим складовим є сучасна діагностична медична техніка.
Дізнатися вартість лікування
Діагностика гострого мієлоїдного лейкозу в Ізраїлі
Спочатку лікар опитує про здоров'я в цілому, попередніх медичних проблемах. Проводить огляд, перевіряючи, чи не збільшені лімфатичні вузли, селезінка та печінка.
Виконується кілька аналізів крові, досліджується кількість різних клітин, здійснюється пошук бластів. Однією з відомих фахівців з лікування раку крові в Ізраїлі є доктор Тавор Сігалу .
Зверніться в TheBestMedic, щоб зв'язатися з лікарем.
Якщо результати аналізів крові є аномальними, гематолог витягує зразок кісткового мозку. Це важливий тест, що дає більше інформації про захворювання, яка необхідна для планування лікування.
Біопсія кісткового мозку
В ході процедури беруть пробу з задньої частини тазової кістки або зрідка з грудини. Перед її початком область знеболюють за допомогою ін'єкції, також може бути запропоновано седативний засіб, що зменшує біль або дискомфорт під час діагностики. Тривалість обстеження становить близько 15-20 хвилин, може проводитися в палаті або в амбулаторному відділенні.
Іноді виконується трепанобиопсия, витягають сегмент кісткового мозку зі збереженням його структури. Для того щоб взяти пробу кісткової тканини, використовують особливий тип голки.
Після процедури на місці вилучення, ймовірно, будуть гематоми і біль протягом кількох днів. У такому випадку застосовують м'які болезаспокійливі засоби.
Отриманий зразок досліджують під мікроскопом, щоб визначити тип гострого мієлоїдного лейкозу. Підраховується кількість бластів, проводять інші тести, які допоможуть підтвердити діагноз.
Різні види гострого мієлолейкозу пов'язані з певними генетичними змінами. Тому такі тести допомагають лікарям вибрати найбільш підходяще лікування гострого мієлоїдного лейкозу та зробити прогноз, як хвороба відреагує.
иммунофенотипирование
Воно передбачає тестування лейкозних клітин антитілами в пошуках специфічних білків на їх поверхні. Иммунофенотипирование допомагає виявити аномальний вид клітин.
цитогенетика
Це дослідження хромосом. Майже всі клітини нашого організму містять хромосоми, в яких розташовані гени, які контролюють всю діяльність клітини. При лейкемії часто виникають мутації в структурі хромосом бластів. Цитогенетичний тест зразка кісткового мозку виявить ці зміни.
Флуоресцентна гібридизація in situ
Цей аналіз використовується, щоб знайти хромосомні зміни, які неможливо виявити за допомогою можливостей цитогенетики.
Плр (полімеразна ланцюгова реакція)
ПЦП – дуже чутливі вид діагностики ХМЛ, здатний знайти мутації в хромосомах, які не можна виявити під мікроскопом. Крім того, його застосовують після лікування, щоб перевірити результативність.
інші дослідження
Також будуть проведені інші види обстежень, які перевірять стан легенів, печінки, нирок і серця. Вони можуть включати рентген грудної клітки, додаткові аналізи крові, елекрокардіограмму і ехокардіографію.
Медичний сервіс «TheBestMedic» надасть допомогу в організації діагностики та лікування гострого мієлоїдного лейкозу в Ізраїлі, в підборі лікарів, медичного закладу та побутового супроводу.
Источник: https://ua.thebestmedic.com/onkogematologiya-lechenie-raka-krovi-v-izraile-lechenie-leykoza-v-izraile/ostryy-mieloidnyy-leykoz